一、前言
化学合成寡核苷酸( Oligonucleotide)药物是指通过化学合成方法制备的具有特定序列和功能的短链核酸药物,通常由十几个至几十个或更长的核苷酸 nt)构成,制备工艺包括固相合成、液相合成以及酶催化片段连接合成等。这类药物通常通过化学修饰技术( 如磷酸骨架修饰、核糖修饰、碱基修饰及与功能性分子偶联等)和/或递送系统( 如脂质纳米粒等)提高其体内稳定性或靶向性。寡核苷酸药物为近年来备受关注的研发领域,ICH 等国际通用技术指南并未完全将其纳入适用范围。为推动寡核苷酸药物行业的发展,助力该类药物的开发与评价,特制定本指导原则。本指导原则适用于反义寡核苷酸 Antisenseoligonucleotide,ASO),小干扰 RNA( small interfering RNA,siRNA)核酸适配体 Aptamer)等化学合成寡核苷酸创新药物的上市申请,不包括 mRNA 等生物合成的核酸药物、抗体偶联核酸药物等。对于寡核苷酸药物的临床试验申请及仿制药申请,可参考本指导原则相关内容。本指导原则仅代表药品监管部门当前的观点和认知,随着科学理论的发展、技术经验的积累以及相关法规的完善,本指导原则的相关内容将不断修订与更新。
二、总体考虑寡核苷酸药物的研发应遵循常规小分子化学药物开发的基本原则,重点结合该类产品的结构和工艺点,进行针对性的研究和控制。可参考 ICH Q8、Q9、Q10、Q11 等指导原则,运用质量风险管理理念,科学利用风险评估工具,从产品设计、生产工艺到质量控制等多维度进行风险识别和评估,制定与产品相适应的整体风险控制策略,并在整个产品生命周期中持续进行药学方面的评估和研究,基于科学和数据不断完善生命周期管理。
相比于小分子化学药物,寡核苷酸药物结构复杂、杂质种类多且结构与终产品类似、精制纯化以及分析手段有限,因此仅通过终产品的质量标准难以完全控制产品质量。建议对合成的起始原料( 如核苷亚磷酰胺等)和中间产品( 如单链寡核苷酸等)开展充分研究和控制,并根据后续工艺参数控制、杂质清除转化研究以及终产品质量控制,建立整体的质量控制策略。
寡核苷酸药物类型众多,其结构特点有所不同。应针对不同类型产品制定针对性的研发策略,如对于采用功能性化学修饰的寡核苷酸类产品应重点对偶联物、偶联位点等进行研究和控制;对于采用载体递送系统的寡核苷酸药物,则应对递送系统( 载体)选择、递送效率、微观形态表征及其他制剂关键质量属性等方面进行全面研究,制定合理的控制策略。
基于寡核苷酸基本组成单元的结构相似性和生产工艺 如固相合成)的平台技术成熟性,寡核苷酸药物的生产、质量控制及稳定性方面的先验知识和平台经验对该类产品的开发具有一定的借鉴意义,因此可用于产品的风险评估、不同临床阶段药学控制以及可比性研究等。寡核苷酸类产品质量可能受原料药起始原料、生产工艺、生产设备、批量、制剂处方工艺等影响,开展关键临床试验后,建议尽量避免不必要的药学重大变更,建议商业化生产拟定的原料药生产工艺、制剂处方工艺等与代表性批次( 如关键临床试验批)尽量保持一致。考虑到寡核苷酸药物开发难度相对较大,并且新技术、新方法的应用带来新的挑战,鼓励注册申请人针对化学合成寡核苷酸药物开发中的重要技术问题尽早与药品监管部门进行沟通和交流。
三、原料药
(一)物料控制
1. 起始原料
应参考 ICH Q11 及其相关问答合理指定起始原料,并全面论述选择合理性。常见的起始原料包括核苷亚磷酰胺( 含预加载核苷酸的固相载体)和非核苷酸部分。应尽量避免使用人或动物源的物料作为起始原料,如必须使用时,应说明传染性海绵状脑病 TSE/BSE)的安全性。
1.1核苷亚磷酰胺
根据寡核苷酸药物的基本组成单元,通常选择受保护的核苷亚磷酰胺作为起始原料。应与供应商接洽,充分了解起始原料的生产工艺和相关控制信息,开展起始原料的杂质研究,结合各类杂质在后续化学反应中的传递、转化和清除情况,评估杂质对终产品质量的影响,制定合理的控制策略。起始原料质量控制项目通常包括:性状、鉴别、含量、杂质、纯度、水分和残留溶剂等。起始原料中部分杂质( 如可参与寡核苷酸链反应循环的杂质)通常会在最终的原料药中持续存在,且下游处理和纯化步骤通常无法完全去除,因此应对此类杂质重点关注并在起始原料的质量标准中进行充分控制。预加载一个核苷酸的固相载体可作为一个整体被指定为起始原料,应结合负载前游离核苷酸、固相载体的质控信息,建立合理的质控策略。
1.2非核苷酸起始原料
用于寡核苷酸的偶联或衍生的非核苷酸部分,如 N-乙酰半乳糖胺( GalNAc),聚乙二醇( PEG)、脂肪酸等,如证明合理亦可以作为起始原料,应关注其质量对终产品关键质量属性的影响,制定合理的质量控制策略。常见质量控制项目包括性状、鉴别、水分、残留溶剂、含量、杂质和纯度等,建议对可参与后续反应的杂质进行风险评估和研究,制定相应的杂质限度。需要特别说明的是部分创新的非核苷酸起始原料( 如新型 GalNAc 产品)并非市售化学品,一般具有结构复杂、合成步骤多、质控难度大等特点,其引入的杂质与核苷酸偶联的风险较高,因此不宜作为起始原料进行控制,建议进一步考虑前延生产工艺。
2.其他物料
寡核苷酸生产所使用的其他物料,包括固相载体、溶剂和色谱填料等,应根据其在生产过程中的作用及对终产品质量的影响,制定合理的质量控制策略。对物料中可参与或影响寡核苷酸合成反应的其他物质或成份,应重点研究并合理控制,如偶联步骤中使用物料的残留水分。固相载体( 非预负载载体)是固相合成的关键物料,常用的载体包括可控孔径玻璃 CPG)和聚苯乙烯树脂。载体的质量控制指标主要包括性状、鉴别、粒径和负载量等。对于 CPG,需检查孔径;对于聚苯乙烯树脂,需关注孔径、膨胀体积等。
(二)生产工艺
1.合成工艺
1.1固相合成工艺
寡核苷酸通常采用固相合成工艺制备,通过自动合成仪在功能化固相载体上进行,典型工艺过程为以固相载体上相应基团( 羟基或预连接第一个核苷酸的羟基)为起始,以脱保护、偶联、氧化/硫代、封端 如适用)等 3~4 个步骤为一个循环,经多次循环,将核苷亚磷酰胺单体沿 3’至 5’方向逐一连接成寡核苷酸链,通过脱保护反应( 如氨解反应)将寡核苷酸链与固相载体裂解并脱除保护基团,然后进一步纯化得到单链寡核苷酸。应对单个循环的每个步骤进行详细描述,包括起始原料、试剂、溶剂、反应时间、温度、当量和浓度等。对于双链寡核苷酸还涉及两条单链寡核苷酸退火步骤,应对退火条件进行详细描述( 例如缓冲液组成、时间、温度等)。对于制备偶联或衍生修饰的寡核苷酸( 如 GalNAc 修饰产品),偶联的分子可以在固相合成前、固相合成完成后、纯化后引入,应研究确定偶联步骤的详细工艺( 例如温度、时间、偶联试剂用量等)。合成寡核苷酸通常使用色谱等技术进行纯化,应明确组分收集、组分合并策略,建立纯化步骤中过程控制标准;如涉及副馏分的纯化,需制定相应的纯化策略,至少包括纳入组分的要求、纯化条件及组分合并的要求等。根据 GMP 相关要求,特别注意应采取适当措施防止交叉污染;色谱柱性能( 如有效塔板数、分离度、堵塞情况等)需符合要求,建议在重复使用前进行必要的性能控制。如果存在任何浓缩步骤( 例如真空蒸发、超滤),则需要对其进行研究,确定具体的工艺参数和控制要求。原料药生产批量受固相合成、分离纯化设备影响较大,需注意合理选择生产设备。基于设备原因需进行亚批拆分或合并操作的,应明确原则以及拆分或合批后批次产品的质量标准。现阶段,原料药以固体( 冻干粉)形式存在是常见的可接受做法。建议慎重开发溶液形式存在的原料药用于制剂生产,如确需选择,请提前与监管机构进行沟通确认。
1.2其他生产工艺
采用其他寡核苷酸制备技术,如液相合成、酶催化片段连接合成等工艺时,需高度关注额外引入的风险( 如偶联效率下降、酶反应引入不同类型杂质等),制定充分的控制策略。
2.关键步骤和中间产品
应根据 ICH Q9~11 进行生产工艺的开发,合理界定关键工艺步骤及工艺参数、明确过程控制和中间产品控制。
2.1关键步骤
根据固相合成法特点,关键步骤可能包括脱保护、偶联、氧化/硫化、封端、裂解、分离纯化、浓缩、干燥、退火( 如适用)和冻干 如适用)等。
2.2中间产品
中间产品可能是裂解后粗品、浓缩液、偶联前的寡核苷酸、退火前的单链寡核苷酸、冻干前的样品等。需合理制定中间产品内控标准,如鉴别、含量、纯度/杂质等质控指标,应建立合理的分析方法并对分析方法进行必要的验证。如涉及采用液相合成、酶催化片段连接等工艺,可将工艺中的短寡核苷酸片段作为中间产品进行控制,控制项目一般包括鉴别、水分、立体构型、纯度、杂质( 重点关注可能引入到终产品中的杂质,如截短或缺失片段等)、含量等。建议对中间产品的贮藏条件和暂存时限进行研究,贮藏条件和暂存时限应有稳定性数据支持。
3.工艺验证
寡核苷酸的工艺验证流程遵循一般化学合成药物的工艺验证原则。注意对于重复使用的物料( 如制备色谱柱)应进行适当的验证。建议采用商业生产规模进行工艺验证。
4.生产工艺开发
通过工艺风险评估和工艺特性研究,明确工艺参数对产品质量的影响,制定相应的控制措施。固相合成工艺采用相对固定的合成设备和工艺过程,应结合目标产品结构特点、关键质量属性等,合理设定工艺参数( 如投料量、反应时间、溶剂用量等)和相应的过程控制要求。在对原料药杂质谱进行全面评估和分析的基础上,结合生产设备能力,确定分离纯化工艺及控制参数。在论证合理的情况下,可参考相近产品( 如寡核苷酸修饰、寡核苷酸链长度等相似的产品)的先验知识。
(三)特性鉴定
1. 结构确证
应通过多种技术手段,如质谱 MS)、核磁共振波谱 NMR)、紫外光谱( UV)、红外光谱( IR)和圆二色谱( CD)等,对寡核苷酸结构和基本特性进行全面表征,包括对一级和/或高级结构的确认。寡核苷酸一级结构应重点确认核苷酸序列,包括明确碱基、核糖和骨架的组成及核苷酸的连接位点、反离子等。常见的表征方法包括:可采用高分辨质谱或质谱联用技术( 如液相色谱-串联质谱 LC-MS/MS)、酶解液相色谱-质谱联用 Enzyme LC-MS)、失效序列分析等)测定寡核苷酸的分子量和序列;可采用 NMR( 包括 31P-NMR、19F-NMR)研究碱基、核糖和骨架的组成及连接位点;另外,可采用元素分析测定碳、氢、氮、氧、硫等元素的含量;可通过离子色谱法、原子吸收光谱法( 火焰光度法等)或电感耦合等离子体发射光谱法等对反离子 如钠离子)进行定量确认。寡核苷酸的高级结构一般包括二级结构( 如可能存在的双螺旋结构)和三级结构( 如适配体的空间结构)。常见的表征方法包括:可采用变性/非变性色谱法对单链或双链寡核苷酸进行区分,可采用紫外熔解曲线分析法测定解链温度( Tm值)等;可采用 CD、傅里叶变换红外光谱( FTIR)、NMR、沉降速率-分析超速离心 SV-AUC)等方法进行高级结构表征。对于具有三级结构的寡核苷酸,可采用近紫外圆二色谱Near-UV CD)法进行三级结构表征。需关注寡核苷酸的立体化学,包括核苷亚磷酰胺起始原料的立体化学纯度,以及在寡核苷酸合成过程中潜在的异构化倾向。对于具有硫代磷酸二酯键的寡核苷酸,由于键合的磷原子是手性的,在偶联反应中会产生 2n个非对映异构体的混合物( n 为硫代磷酸酯键的数目),需要评估非对映异构体的分布及其重现性,同时关注立体化学对生物/药理活性的影响。立体化学检测常用的方法包括 31P-NMR、阴离子交换色谱( AEX-HPLC)、离子对反相色谱( IP-RP-HPLC)、CD 等。部分具有偶联结构的原料药,如完整原料药结构确证困难,可对偶联和非偶联部分分别进行结构表征,确定偶联和非偶联部分的结构,并证明偶联位点的专属性。对于 siRNA 等双链寡核苷酸,应分别对单链 正义链、反义链)以及双链进行特性鉴定。
2.理化性质
包括但不限于性状、含水量、酸碱度、摩尔吸光系数、在不同介质中的溶解度、吸湿性、等电点、固体形态、热力学性质( TGA、DSC)等。双链寡核苷酸、适配体应关注 Tm值。
(四)质量研究与控制
1.质量标准
可参照 ICH Q6A 的基本原则,根据寡核苷酸的结构特点、制备工艺、理化性质合理设定质量研究项目。原料药质量研究和控制的典型项目一般包含性状、鉴别、酸碱度、纯度和杂质、反离子含量、水分、细菌内毒素、微生物限度、含量等。应对残留溶剂、元素杂质进行风险评估,制定合理的控制策略。建议参考国内外相关技术要求开展致突变杂质 包括亚硝胺杂质)的风险评估和研究,必要时在质量标准中进行控制。对于双链寡核苷酸,质量标准在常规检测项目基础上,通常还应包含针对双链特征的鉴别项,如非变性HPLC、Tm等。建议同时使用非变性方法 以测量单链残留量)和变性方法测试纯度。对于适配体等具有高级结构的寡核苷酸,通常需进行生物活性测试。
2.分析方法
2.1 分析方法开发
对于水分、细菌内毒素和微生物限度等常规检测项目,应参考国内外药典的分析方法进行测定。针对寡核苷酸的结构和理化特性的特殊检测项目应建立特定的分析方法。鉴别建议采用不同原理的方法进行鉴别。常见的鉴别如下:分子量鉴别:实测分子量应与理论分子量一致。通常采用液相色谱-质谱联用 LC-MS)、高分辨质谱等方法。序列鉴别:核苷酸序列应与理论序列一致。可采用质谱进行碎片序列和/或失败序列分析、紫外熔解曲线分析测定Tm 如适用)等,确证寡核苷酸整体序列。保留时间鉴别:采用 HPLC 法对比供试品溶液与对照品溶液主峰保留时间,应保持一致。此外,还可对反离子、特殊寡核苷酸修饰 如 2’F 取代)进行相应鉴别。对于双链寡核苷酸,应分别证明单链与理论结构保持一致,并证明两条单链结合状态。可考虑采用非变性色谱、Tm检测确定结合状态、通过质谱确定两条单链分子量。具有高级结构的寡核苷酸 如适配体),还应关注高级结构的鉴别。纯度和杂质由于部分寡核苷酸杂质的结构、性质与主成份较为相似,杂质分离难度较大。建议开发合适的分析方法尽可能实现杂质分离。推荐采用多种不同分离原理的分析方法,包括 IPRP-HPLC、离子交换色谱 IEX-HPLC)、LC-MS、毛细管电泳 CE)、分子排阻色谱 SEC)、亲水作用色谱 HILIC)等,以及不同检测器的分析方法 如 UV 和 MS 检测器)进行杂质检查,以改善杂质的分离、鉴定和定量。建议选择富含杂质的样品进行杂质分析方法的研究和确认,如纯化步骤前的粗品、不同工艺参数/纯化条件制备的样品、强制破坏或影响因素及加速试验样品等。对经充分研究仍无法有效分离的寡核苷酸杂质,可考虑按保留时间等对杂质进行分组控制,此时应充分论证分组的合理性,并尽量确定各分组内杂质的组成。对于双链寡核苷酸,一般采用非变性方法 如非变性 IP-RP-HPLC、SEC、CE等)对单链的残余量进行分析和控制,采用变性方法考察纯度和杂质。
立体异构体
立体异构体检查可考虑采用的检测方法包括色谱法 如AEX-HPLC、IP-RP-HPLC、HILIC)、离子淌度质谱 IM-MS)、CE、NMR、CD 和基于酶裂解反应的检测方法等。如无法实现所有异构体的分离,需评估立体异构体的分布,必要时进行合理控制。
含量应明确规定含量限度及其计算方法。含量可采用 UV、HPLC、LC-MS 等方法进行测定,通过与已知纯度和浓度的对照品比较或基于摩尔吸光系数根据吸光度进行定量。建议首选专属性较强的方法 如 HPLC 法)。冻干的寡核苷酸原料药建议含量以无水物标示。
体外生物活性
对于 ASO 或 siRNA 等结构相对简单的寡核苷酸,其生物活性通常由其序列结构控制,鼓励开发体外生物活性方法,用于可比性等研究。一般无需将体外生物活性纳入常规放行检测项。对于适配体或其他具有三维结构的寡核苷酸,其作用机制依靠独特的空间结构、特异性结合靶分子而发挥生物活性,通常需建立细胞试验分析方法和其他生物分析方法进行体外生物学活性测定和控制。如需进行化学修饰对生物靶标的结合活性检测,可考虑采用表面等离子共振 SPR)、酶联免疫吸附试验 ELISA)、荧光偏振 FP)等方法进行研究。
2.2 分析方法验证
原料药质量控制的分析方法应按照 ICH Q2、Q14 及国内外药典等相关指导原则进行方法验证。验证时关注分析方法的专属性,提供证明寡核苷酸相关杂质与主峰有效分离的色谱图和相关质谱数据。应加强方法的耐用性考察,充分考虑色谱柱、溶剂及其他色谱条件等的影响。分析方法的灵敏度应满足检测需要,例如,通常情况下,质谱法检测寡核苷酸相关杂质时,分析方法灵敏度应达到 0.1%~0.3%。
3. 杂质分析
建议结合起始原料和寡核苷酸的合成工艺、中间产品和目标产物的降解途径及降解产物研究,全面分析和表征寡核苷酸的杂质。考虑到相关杂质结构复杂且与目标产物结构相似、现有分析技术有限等,建议结合先验知识以及文献资料等,尽可能对主要存在的寡核苷酸杂质进行表征。
3.1 寡核苷酸相关杂质
寡核苷酸相关杂质来源主要包括起始原料引入、生产工艺过程中形成、生产或贮藏过程中降解产生。下表列举了常见的寡核苷酸相关杂质及其可能的来源:
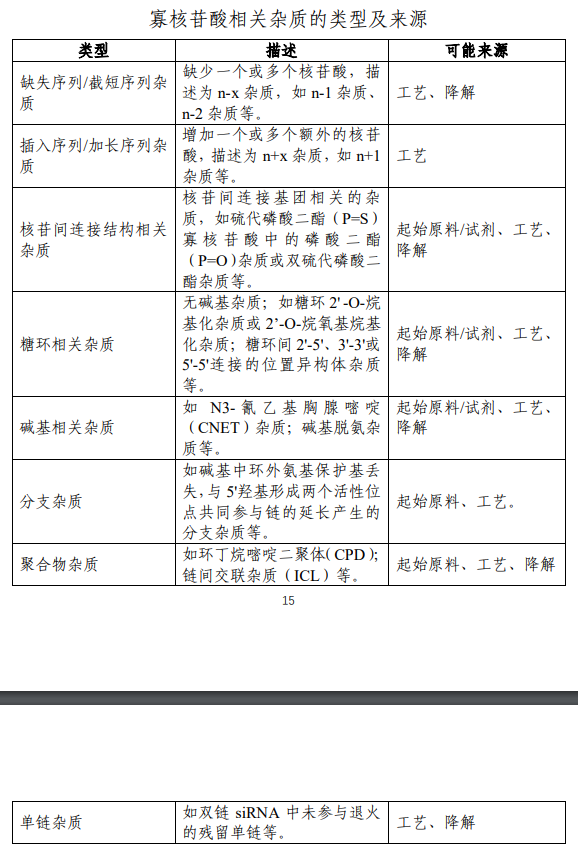
寡核苷酸相关杂质的控制:
通常,寡核苷酸相关杂质可接受的报告限为 0.2% 部分结构复杂、分子量大的杂质可基于分析方法的定量限适当调整)、鉴定限为 1.0%、界定限为 1.5%。对于超过界定限的杂质,应有界定数据支持。寡核苷酸相关杂质可根据杂质的结构分为四个不同的类别,不同类别杂质的相关界定数据要求如下:I类杂质为与主要代谢物结构相同的杂质,如:主成份核酸 3'或 5'端缺少一个或多个核苷酸的杂质、双链寡核苷酸的单链杂质、偶联寡核苷酸中的游离寡核苷酸杂质等。此类杂质即使含量超过界定限也无需额外的安全性评估。II 类杂质为仅含天然存在的核酸结构的杂质,如:硫代磷酸二酯被天然磷酸二酯代替的杂质。此类杂质即使含量超过界定限也无需额外的安全性评估。III 类杂质为由活性成份寡核苷酸的序列变体组成,如:链内缺少核苷酸或添加核苷酸的 n-1 或 n+1 杂质 不在序列的 3'或 5'端)、由脱氨引起的尿嘧啶 或胸腺嘧啶)取代胞嘧啶 或 5-甲基胞嘧啶)的降解产物。通常可将此同类杂质识别并量化为一组。对于含量超过 1.5%的一组杂质,则每个序列的杂质需进行归属研究,超过 1.5%的单个序列还需要进行安全性评估。对于其他可能引起安全性担忧的杂质 如与其他靶点杂交且产生药理作用的杂质),即使其含量未超过1.5%,也建议进行合理的安全性评估。IV 类杂质为含有活性成份以外的核苷酸或非天然核酸结构元素的杂质,如:无碱基杂质。若此类杂质含量超过 1.5%,建议优化生产工艺来降低杂质水平,如不能降低,需进一步进行安全性评估。关于杂质界定的总体策略可参考附件的决策树。对于上述不同类别的杂质,应根据安全性评估数据 如涉及),同时考虑相关文献或指导原则、历史批次数据和稳定性数据,合理制定杂质的限度。对于与其他功能分子偶联的寡核苷酸药物,需关注功能分子中可偶联杂质 例如 GalNAc 中脱乙酰基、糖环水解等杂质)与寡核苷酸偶联的风险。
3.2 非寡核苷酸杂质
寡核苷酸常规生产工艺 如固相合成中的多次洗涤、制备纯化、超滤等)通常对小分子杂质具有较高的清除能力,针对合成使用的有机溶剂、试剂以及生产过程中的小分子副产物、残留溶剂、元素杂质、配体、保护基等,可根据其清除能力和实际检测数据等评估其残留风险,并按相关指导原则进行控制。对于致突变杂质 包括亚硝胺杂质),建议关注包括起始原料可能引入的亚硝胺杂质,寡核苷酸在合成过程中使用的脱 DMT 4,4'-二甲氧基三苯甲基)试剂、氨解试剂、核苷亚磷酰胺的临时保护基团等发生反应生成的副产物,或涉及偶联工艺时偶联物自身或偶联过程中可能形成的致突变杂质,酌情控制。
(五)对照品
一般情况下,需建立寡核苷酸原料药及关键中间产品的对照品。双链寡核苷酸的对照品一般包括正义链、反义链和双链寡核苷酸本身。对于用于单链寡核苷酸鉴别 例如 Tm)的互补链寡核苷酸,也应建立对照品。对于质量标准中规定的特定杂质建议通过定向合成方法制备代表性杂质对照品,也可通过工艺优化或分离纯化获得,其纯度应满足分析要求。对照品应明确来源 例如,根据商业工艺合成的批次)、制备和标定信息,及对照品批次的表征方法和结果。寡核苷酸对照品应明确贮藏条件及有效期。
(六)稳定性
稳定性研究应遵循 ICH 稳定性相关指导原则。结合工艺开发过程中发现的药物不稳定因素,在稳定性考察中重点关注。稳定性研究项目应包括在贮藏过程中容易发生变化并可能会影响质量、安全性和/或有效性的关键质量属性。稳定性考察中应特别关注降解杂质,例如氧化杂质、脱氨杂质、无碱基杂质 脱嘧啶、脱嘌呤)等。对于吸湿性粉末,稳定性研究中应考察水分。此外还应关注和考察寡核苷酸是否发生聚集现象。
四、制剂
寡核苷酸药物大多具有易被酶解、脂溶性差等特点,口服生物利用度较低,通常以注射途径给药 如皮下注射、静脉注射、鞘内注射等),因此本节内容主要根据注射剂进行阐述。随着技术的发展,寡核苷酸药物亦可能被开发为其他制剂类型。对于其他给药途径 剂型)的产品,应结合制剂特点,参照各剂型相关指导原则开展研究和控制。
(一)产品开发
1. 剂型及递送系统
寡核苷酸药物通常开发为普通注射剂,包括注射液、注射用无菌粉末。部分品种基于临床需要,可开发为具有载体递送系统的特殊注射剂,如脂质纳米粒等。
2. 处方工艺开发
2.1 处方开发
在常规制剂开发基础上,结合原辅料相容性研究结果,关注辅料是否会引起寡核苷酸药物杂质谱的变化、非预期高级结构和聚集体的形成及其他对产品质量和安全性的潜在影响。
2.2 生产工艺开发
生产工艺开发时应充分了解影响寡核苷酸药物稳定性的各种因素,如 pH 值、光照、温度等,在拟定生产工艺中应尽量避免敏感因素的影响并制定合理的控制策略。应参照相关指导原则根据研究数据合理选择灭菌/无菌生产工艺。
2.3 相容性等研究
应按照相关指导原则的要求开展包材相容性、生产组件相容性、包装系统密封性、配伍稳定性等相关研究。
2.4 具有载体递送系统的特殊注射剂
对于脂质纳米粒等具有载体递送系统的注射剂,处方开发应重点关注功能性辅料 包括脂质、非脂质辅料)的来源、理化特性、生产工艺、质量控制、稳定性等,以及载体递送系统对活性成份的保护作用、递送效率等的影响,注意对制剂关键质量属性 如粒径分布、形态和结构、表面电位、包封率、杂质残留和稳定性等)进行考察,充分论证各辅料的选择依据及处方合理性。工艺开发时应重点关注药物包封步骤、纯化步骤和除菌过滤等对制剂关键质量属性的影响。
(二)生产工艺
1.生产工艺
寡核苷酸药物制剂的生产工艺通常包括配液、除菌过滤、灌封、包装等步骤。应结合工艺开发研究及生产设备放大的实际控制能力,合理设定工艺参数。对于脂质纳米粒等特殊注射剂,需进一步严格工艺控制,载体递送系统的形成步骤应作为关键步骤,并加强中间产品的质量控制。
2.工艺验证
商业化生产工艺确定后,建议采用商业化生产工艺及规模在商业化生产场地进行工艺验证。考虑到寡核苷酸产品的工艺复杂性和产品变异性,应结合产品开发及风险评估,合理选择工艺验证参数,制定工艺验证方案,验证批次通常不少于三批。
3.批量
应注意识别从临床规模放大至商业化规模生产过程中的风险并制定控制策略。由于脂质纳米粒等特殊制剂的复杂性,其生产规模变化导致的生产设备及参数的变化可能产生大量不可预期的风险,建议拟定商业化生产批量与关键临床试验样品的生产批量保持一致。
(三)质量研究与控制
应参照注射剂相关指导原则开展寡核苷酸注射剂质量研究。对于脂质纳米粒等纳米载体递送系统,建议同时参考《纳米药物质量控制研究技术指导原则 试行)》、《脂质体药物质量控制研究技术指导原则》 如适用)等国内外相关指导原则开展研究。
1.质量标准
可参照 ICH Q6A 的基本原则制定寡核苷酸制剂的质量标准。质量研究和控制的典型项目一般应包括注射剂常规控制项目,如性状、鉴别、澄清度与颜色、pH 值、降解杂质、渗透压摩尔浓度、可见异物、不溶性微粒、细菌内毒素、无菌、含量等。如为注射用无菌粉末,还应包括水分、复溶时间等。在注射剂常规项目的研究基础上,应结合原料药、偶联情况、辅料以及剂型 如载体递送系统)和包材特性等合理设定有针对性的质量研究和控制项目。对于脂质纳米粒等特殊制剂,应关注功能性辅料 脂质、非脂质)的鉴别和含量、脂质相关降解产物、纳米相关特性指标 如结构形态、粒径及粒径分布、表面性质、包封率、释放度)等研究。对于涉及高级结构并影响其生物活性的寡核苷酸药物 如适配体),应考虑进行高级结构和生物活性等检测。如果在成品生产和/或贮藏过程中可能发生聚集/聚合,一般应将相关指标 如聚集体、聚合物、高级结构等)纳入成品质量标准进行控制。
2.分析方法
建议结合制剂处方工艺,参考原料药制定制剂的质控分析方法。如经确认方法适用,部分检测项目可直接采用与原料药相同或相近的分析方法,如鉴别、纯度、杂质、含量、生物活性等。制剂杂质的分析方法,在原料药的杂质分析方法基础上,关注制剂降解杂质、原辅料相互作用杂质的分离检出能力,必要时进行优化。对于制剂中的潜在聚集体杂质,应采用合理的分析方法进行检测,如 SEC 法。
对于脂质纳米粒等特殊制剂,应充分考虑分析方法的适用性和不同方法之间的互补性,在此基础上优选专属性高、耐用性好的分析方法作为最终质量标准中的分析方法。采用非药典方法时,应明确分析方法的测定参数,确保可操作性及重现性。对制剂关键考察项目的分析方法应进行完整的方法学验证。鼓励采用杂质对照品进行降解杂质分析方法验证。
3. 杂质分析
应重点研究制剂工艺相关杂质 包括原料药与辅料和/或内包材的反应产物等)、制剂的降解杂质 包括可能出现的聚集体杂质)。应进行元素杂质、致突变杂质 包括亚硝胺杂质)的评估和控制。建议根据制剂强制降解、影响因素等试验考察制剂高温、光照、不同 pH 值条件下降解情况,全面了解制剂降解途径及降解杂质。常见降解杂质包括氧化杂质 如硫代磷酸酯 P=S)寡核苷酸氧化产生的磷酸二酯 P=O)杂质)、热降解杂质 如磷酸二酯键水解产生的断裂寡核苷酸序列、碱基脱氨反应使胞嘧啶 C)转化为尿嘧啶 U)、腺嘌呤 A)转化为次黄嘌呤 I)杂质)、酸碱降解杂质 如酸性条件下脱嘌呤或脱嘧啶反应产生的无碱基杂质;碱性条件下核苷酸链水解产生的断裂寡核苷酸序列)、水解杂质 如断裂寡核苷酸杂质、糖基修饰杂质、糖基脱落杂质)、光降解杂质 如碱基氧化、环化、嘧啶碱基发生二聚化反应形成的二聚体杂质)。对于制剂的寡核苷酸相关杂质,通常可接受的报告限为0.2% 部分结构复杂、分子量大的杂质可基于分析方法的定量限适当调整)、鉴定限为 1.0%、界定限为 1.5%。
(四)稳定性
稳定性研究应遵循 ICH 稳定性相关指导原则。稳定性研究项目应考察关键质量属性,特别关注降解杂质,例如氧化杂质、脱氨杂质、无碱基杂质 脱嘧啶、脱嘌呤)等。此外还应关注和考察寡核苷酸是否发生聚集现象。
五、药学可比性研究
寡核苷酸药物的开发遵循创新药研发的一般规律,可能面临各类药学变更的情形,应结合所处的产品开发阶段、变更的性质、先验知识和经验等进行风险评估。根据风险评估的结果决定需要进行的可比性研究内容。药学可比性研究的目的在于证明药学变更前后产品的关键质量属性一致。通常,可比性研究可能包括如下方面。
(一)结构确证
通常,发生可能影响产品结构的生产工艺变更(如起始原料供应商变更、固相合成工艺变更、批量放大等),需对变更前后生产的产品进行结构确证及比较。除常规结构确证项目外,对于双链寡核苷酸,应进行双链杂交状态确证研究,采用的方法包括 FTIR、紫外熔解曲线分析 测定 Tm)等。对于存在高级结构的寡核苷酸,应进行高级结构对比研究,采用的方法包括 CD、DSC、SEC、SV-AUC 等,必要时还需要测定生物活性进行比较。
(二)质量对比研究
通常应对质量标准控制项目和产品其他关键质量属性进行检测,如原料药含量、杂质、反离子等;制剂含量、杂质、异构体、释放度 如有)等。质量对比研究需重点关注产品杂质谱,应充分评估变更对杂质谱可能产生的影响,建议使用不同分离原理的分析方法进行深入的杂质对比研究,检测方法需能够涵盖寡核苷酸的完整杂质谱 必要时可采用补充方法进行额外的杂质检测)。如变更后产品检测到新增寡核苷酸杂质,根据杂质水平,对于超鉴定限的杂质需进行杂质结构确证;对于超过界定限的杂质,可遵循上文所述的杂质分类原则评估是否需进一步进行安全性评估。应比较变更前后产品的立体异构体特征,在立体异构体检测的基础上,建议关注可能影响产品立体化学的物料质量如核苷亚磷酰胺起始原料、载体固定的寡核苷酸、催化剂和溶剂)、生产工艺( 如柱层析色谱条件)参数,以论证变更前后的生产工艺所制备的产品立体异构体分布相似。
(三)稳定性对比研究
一般需进行变更前后产品的稳定性研究。重点关注可能受到变更影响的质量属性。如果原料药的药学变更可能影响到制剂的生产工艺或产品质量,通常需要对原料药及其制剂同时进行评估。当药学评估结果表明变更会对产品的安全性或有效性产生风险时,应进一步评估并考虑开展非临床和临床桥接研究。
六、参考文献
[1] 国家药品监督管理局药品审评中心.《化学药物杂质研究技术指导原则》[EB/OL]. 2005年3月.
https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=d5e37f20dbe191fdaa2e1543a3d82c0c.
[2] 国家药品监督管理局药品审评中心.《创新药 化学药)临床试验期间药学变更技术指导原则》[EB/OL]. 2021年3月.
https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=e1a358fd48693f910793b109794d55ab.
[3] 国家药品监督管理局药品审评中心.《化学药品注射剂与药用玻璃包装容器相容性研究技术指导原则( 试行)》[E
B/OL].2015年7月.
https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=e821b8271ff9f2f205ed425c36f9bd0b.
[4]国家药品监督管理局药品审评中心.《化学药品注射剂包装系统密封性研究技术指南( 试行)》[EB/OL]. 2020年10月.
https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=f01da29a809838c020662f2aca59baa7.
[5]国家药品监督管理局药品审评中心.《化学药品注射剂配伍稳定性药学研究技术指导原则 试行)》[EB/OL]. 2024年6月.
https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=7b860bc7a49e596eb49cfcc04e6b7d38.
[6]国家药品监督管理局药品审评中心.《纳米药物质量控制研究技术指导原则 试行)》[EB/OL]. 2021年8月.
https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=3e60526d467585dc77d35445f04bae5c.
[7]国家药品监督管理局药品审评中心.《脂质体药物质量控制研究技术指导原则》[EB/OL]. 2023年10月.
https://www.cde.org.cn/zdyz/domesticinfopage?zdyzIdCODE=99196333e688523de419ea2ff74910c2.
[8]ICH Q6A: Specfications: Test Procedures and Acce ptance Criteria for New Drug Substances and New Drug P
roducts: Chemical Substances[EB/OL]. Oct 1999.
https://database.ich.org/sites/default/files/Q6A%20Guideline.pdf.
[9]ICH Q8(R2): Pharmaceutical Development[EB/OL].Aug 2009.
https://database.ich.org/sites/default/files/Q8%28R2%29%20Guideline.pdf.
[10]ICH Q9(R1): Quality Risk Management[EB/OL].Jan 2023.
https://database.ich.org/sites/default/files/ICH_Q9%28R1%29_Guideline_Step4_2025_0115_0.pdf.
[11]ICH Q10: Pharmaceutical Quality System[EB/OL].June 2008.
https://database.ich.org/sites/default/files/Q10%20Guideline.pdf.
[12]ICH Q11: Development and Manufacture of Drug Substances (Chemical Entities and Biotechnological/Biologic
al Entities) [EB/OL]. May 2012.
https://database.ich.org/sites/default/files/Q11%20Guideline.pdf.
[13] European Medicines Agency. Draft guideline on the development and manufacture of oligonucleotides: Guide
line on the Development and Manufacture of Oligonucleotides[EB/OL]. July 2024.
https://www.ema.europa.eu/en/documents/scientific-guideline/draft-guideline-development-manufactu
re-oligonucleotides_en.pdf.
[14] D Capaldi, A Teasdale, S Henry, et al. Impurities in Oligonucleotide Drug Substances and Drug Products[J].
Nucleic Acid Ther, 2017, 27(6): 309-322.
来源:CDE
原文下载:![]() 化学合成寡核苷酸药物(创新药)药学研究技术指导原则(试行).pdf
化学合成寡核苷酸药物(创新药)药学研究技术指导原则(试行).pdf
 咨询热线:400-888-1942
咨询热线:400-888-1942




