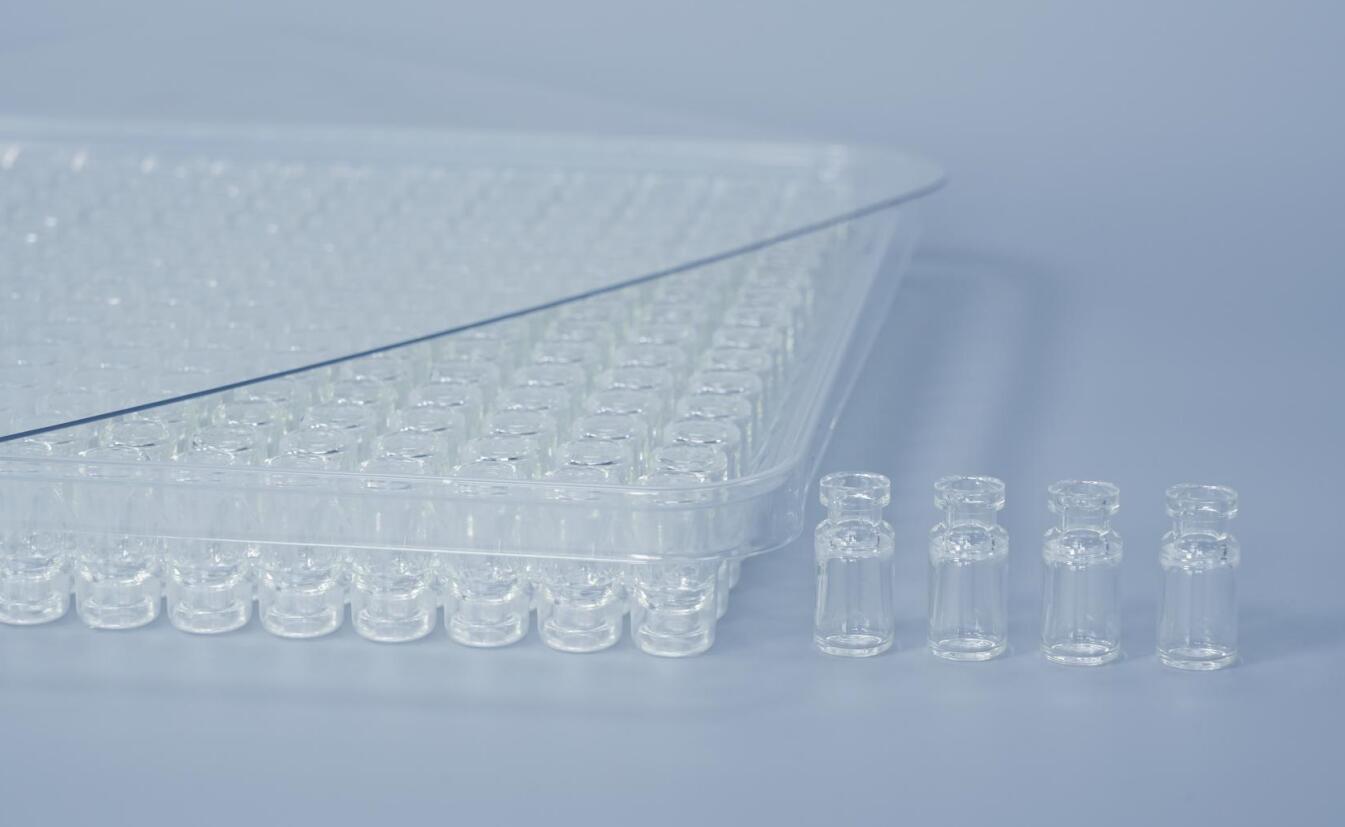
干细胞药物作为革命性的治疗产品,其研发与申报是一项复杂的系统工程。在申报临床试验阶段,药学研究的核心目标是充分证明候选产品的安全性,并为临床试验的顺利开展提供质量可控的样品。其中,包装容器密封系统的选择至关重要,它直接关系到药物在储存、运输及使用过程中的稳定性、无菌性和安全性。本文将结合《人源干细胞产品非临床研究技术指导原则(试行)》等相关技术要求,深入分析干细胞药物IND申报中包装系统需关注的要点,并阐述(环烯烃聚合物)COP西林瓶如何成为满足这些严苛要求的理想解决方案。
COP西林瓶
一、 指导原则对包装系统的核心要求
CDE发布的指导原则为干细胞药物的药学研发提供了明确方向。在包装系统方面,要求可概括为以下几点:
稳定性支持:包装系统必须能够保障干细胞药物在设定的储存条件(如-196°C液氮或-80°C深低温)下,在整个有效期或临床使用期间维持物理、化学和生物学的稳定性。这包括保持细胞活性、防止非预期分化、控制相关杂质水平等。
相容性验证:必须进行包装容器与制剂的相容性研究。这要求评估包装材料与干细胞制剂(包括细胞本身、冻存液中的DMSO等辅料)之间是否发生相互作用,导致材料中的可提取物/浸出物迁移至药液中,或药液中的成分被包装材料吸附,从而影响产品质量或引入安全性风险。
密封完整性保证:对于无法终端灭菌的无菌制剂,包装系统的容器密封完整性 是防止微生物侵入和外源因子污染的生命线。尤其是在经历剧烈的温度变化(如从液氮中取出至室温水浴复苏)后,密封系统必须保持完整,确保无菌状态。
二、 COP西林瓶如何满足关键质量属性
COP材料具有极高的化学惰性和纯度,其表面能低,表现出极低的蛋白吸附特性。这对于干细胞药物至关重要,能最大限度地减少珍贵细胞因子或细胞膜表面蛋白的损失,确保给药剂量的准确性。在与冻存液中常用成分(如DMSO)的相容性方面,COP也表现出优异的稳定性,不易发生反应或释放有害物质,为细胞提供一个洁净、安全的储存环境。
干细胞药物常需在-196°C液氮或-80°C的超低温环境中长期保存。COP材料具备极低的热膨胀系数,且与常用的溴丁基橡胶塞的热收缩性能高度匹配。这意味着在极端低温下,瓶体与胶塞能保持同步收缩,有效避免了因两者收缩率差异过大而产生的微间隙,从而显著降低了液氮或微生物渗入的风险,确保了容器密封完整性在经过多次冻融循环后依然可靠。
COP西林瓶的高透明度(透光率>92%)便于对瓶内药液进行外观检查。其优异的水汽阻隔性能,能有效防止储存期间水分的透过,对于维持冻干制剂或特定浓度细胞悬液的稳定性尤为重要。在进行稳定性研究时,使用COP西林瓶包装的样品,其关键质量属性(如细胞活率、纯度、生物学活性)的数据更能真实反映产品本身的变化,减少了由包装材料引入的干扰变量,为制定科学合理的有效期和储存条件提供了可靠依据。
三、 IND申报中的药学资料准备
在选择COP西林瓶作为包装系统后,在IND申报资料中应提供相应的研究数据和证明:
包装系统基本信息:提供COP西林瓶(包括胶塞、铝盖)的来源、质量标准。
相容性研究数据:提交可提取物和浸出物研究的方案和初步数据,评估在特定储存条件下,从包装材料中可能溶出的物质及其对干细胞药物的潜在影响。
密封完整性验证报告:提供采用物理测试方法验证COP西林瓶在经历极端低温储存和运输后仍能保持密封完整性的数据。
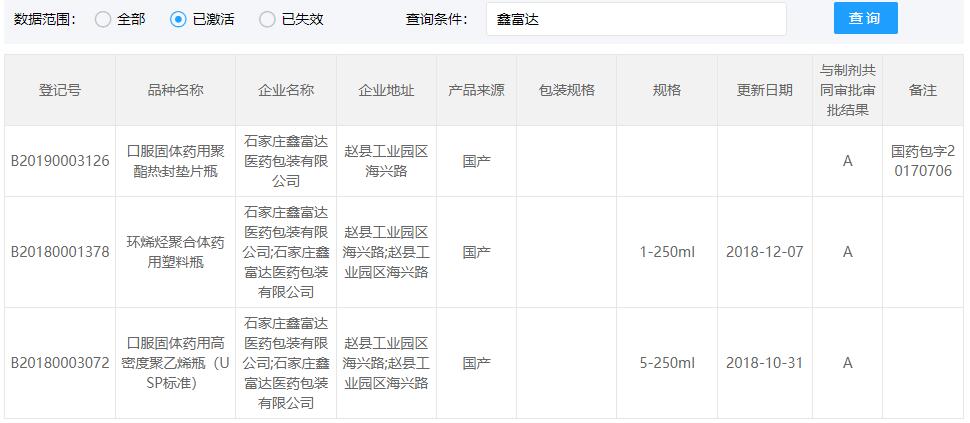
COP西林瓶CDE登记号为A状态
在干细胞药物IND申报的药学研究中,对包装系统的选择绝非小事。以《人源干细胞产品非临床研究技术指导原则》为纲,聚焦于稳定性、相容性、密封完整性三大核心要点,是评估和选择包装方案的关键。COP西林瓶凭借其先天的材料优势,在这三个方面展现出卓越的性能,能够为高价值的干细胞药物提供从生产到临床使用全周期的稳定保护,是助力药物顺利通过IND审评,加速其临床转化的可靠且理想的包装选择。
 咨询热线:400-888-1942
咨询热线:400-888-1942