在2025年新规下,医美企业向COP西林瓶包装的过渡需围绕法规合规、技术适配、供应链管理及成本优化展开系统性升级。以下是基于政策要求与行业实践的全流程解决方案:
一、精准解读新规核心要求,构建合规框架
1. 明确产品分类与认证标准
根据国家药监局《医疗器械产品分类界定结果》,注射用透明质酸钠复合冻干粉被纳入药械组合产品管理,需同时满足药品 GMP 和医疗器械 GMP 标准。企业需确保COP西林瓶通过 USP <661.1> 塑料材料功能性测试、ISO 10993-5 细胞毒性测试(细胞活性≥90%),并控制 17 项基因毒性杂质(检出限≤0.03 μg/mL)。对于三类械字号冻干胶原蛋白,需采用全程无菌包装,内毒素≤0.25 EU/mL,灌装环境达 A 级洁净标准。
COP西林瓶
2. 标签与追溯系统升级
新规要求二类械字号冻干粉需满足《医疗器械唯一标识系统规则》,COP 西林瓶内壁激光打码需耐液氮侵蚀,扫码率≥99.9%。企业应同步更新标签内容,包括新注册证号、追溯码及无菌标识,并通过美团 “放心美” 等平台接入药品追溯码与 UDI 系统,实现全流程验真。
3. 过渡期库存管理
若旧包装库存量大,可向省级药监部门申请过渡期(通常≤6 个月),但需加贴新证号标签覆盖旧信息。建议新证获批前 3 个月启动包装物料切换计划,减少浪费。
二、技术适配与供应链优化
COP西林瓶性能验证
活性成分保护:COP的低水分透过率(<0.01 g・mm/m²・day)可防止冻干粉吸湿结块,透明质酸分子量降解率从玻璃瓶的 15% 降至≤2%;低蛋白吸附性(≤0.05 μg/cm²)可使冻干重组 Ⅲ 型人源化胶原蛋白回收率≥98%。
极端环境稳定性:在-196℃液氮环境下,COP西林瓶体体积变化率≤0.02%,支持 CAR-T 细胞制剂经 10 次冻融循环后破裂率为 0%。某临床级 AAV 载体使用 COP 瓶存储 6 个月后,基因组完整性保持率≥99%,较玻璃瓶组提高 12 个百分点。
灌装工艺升级
COP 西林瓶适配隔离器灌装线,背景环境可降至 D 级,结合全自动撕膜揭盖系统,人员干预频次降低 90%,污染风险<0.1%。企业需评估现有生产线是否需升级至 A 级洁净环境,并引入数字孪生技术优化液氮存储系统的堆码稳定性,将开盖破损率从 0.5% 降至 0.02%。
供应链多元化布局
国内供应商如拓烯科技、无锡阿科力已实现千吨级 COP 量产,日本瑞翁在华工厂产能达 4.76 万吨 / 年。建议选择 CDE 登记号为 A 状态的供应商,确保产品通过关联审评。对于高端产品,可考虑进口瑞翁再生 COP 材料,其与原始树脂质量水平一致,且碳足迹更低。
三、成本控制与风险应对
1. 材料与工艺创新
COP 西林瓶薄壁设计(0.8-1.2mm)可降低原材料用量 30%,搭配超临界 CO₂再生技术,单瓶成本较玻璃瓶仅高 15%,但溢价空间达 300%。例如,某冻干面膜通过 COP包装实现300元/盒的溢价。
2. 合规性风险预控
需建立 COP 西林瓶与医美产品的相容性数据库,涵盖不同 pH 值(如>10 的碱性药物)、渗透压条件下的溶出物检测。对于常温型冻干肉毒素,需验证其在 18 个月常温保存下的活性保留率>95%,并通过临床数据证明复溶后弥散度降低 20%。
3. 员工培训与应急预案
针对无菌灌装、激光打码等新工艺,需开展分级培训:生产人员需掌握隔离器操作与 A 级环境控制,质量人员需熟悉 USP <661.1> 测试方法。同时,建立供应链备份机制,与 2-3 家供应商签订优先供应协议,应对可能的原材料短缺。
四、长期战略与行业协同
1. 环保与可持续发展
COP材料可通过超临界 CO₂再生技术循环利用,残留 DNA 片段≤0.1 ng/cm²,满足 mRNA-LNP 制剂的洁净度要求。企业可申请 ISO 14001 环境管理体系认证,提升品牌绿色竞争力。
2. 行业标准参与
积极参与《生物制品包装系统密封性指南》等新规制定,推动COP西林瓶在极低温D值验证(微生物侵入概率≤10⁻³)与快速升温复融(60℃/2 min)场景的应用标准化。
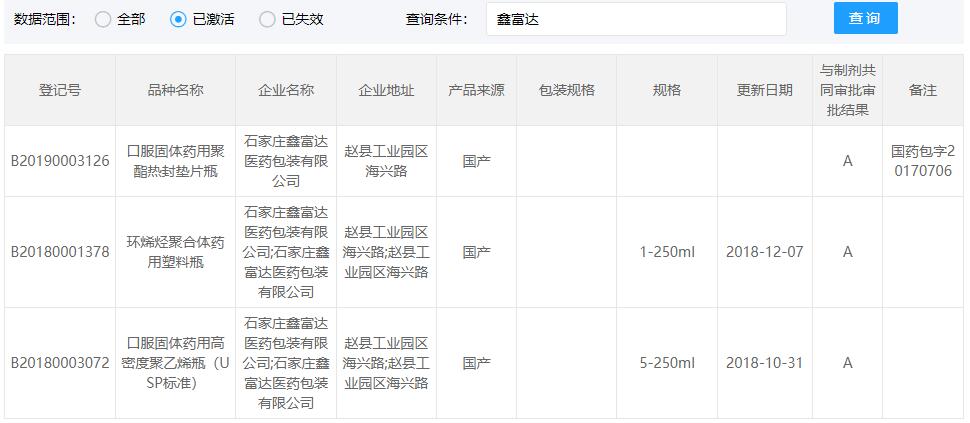
COP西林瓶CDE登记号为A状态
3. 临床数据驱动市场
联合医疗机构开展临床研究,例如通过COP西林瓶包装的玻尿酸填充剂在植入后骨融合率提升30%、过敏率仅为传统产品1/5的数据,强化市场对新材料的信任。
五、实施路径与时间节点
阶段 | 关键任务 | 时间节点 |
合规准备 | 完成 COP 西林瓶 CDE 关联审评,启动生产线洁净度升级改造 | 新规生效前 6 个月 |
试产验证 | 开展 3 批次中试,验证活性成分保留率、密封性及标签追溯系统 | 新规生效前 3 个月 |
全面切换 | 旧包装库存消化完毕,新包装正式投产,同步更新标签与追溯系统 | 新规生效后 1 个月 |
持续优化 | 收集临床反馈,迭代包装设计,申请环保认证 | 长期 |
通过以上策略,医美企业可在满足 2025 年新规要求的同时,借助COP西林瓶的技术优势提升产品附加值,实现合规性与商业价值的双赢。
 咨询热线:400-888-1942
咨询热线:400-888-1942






