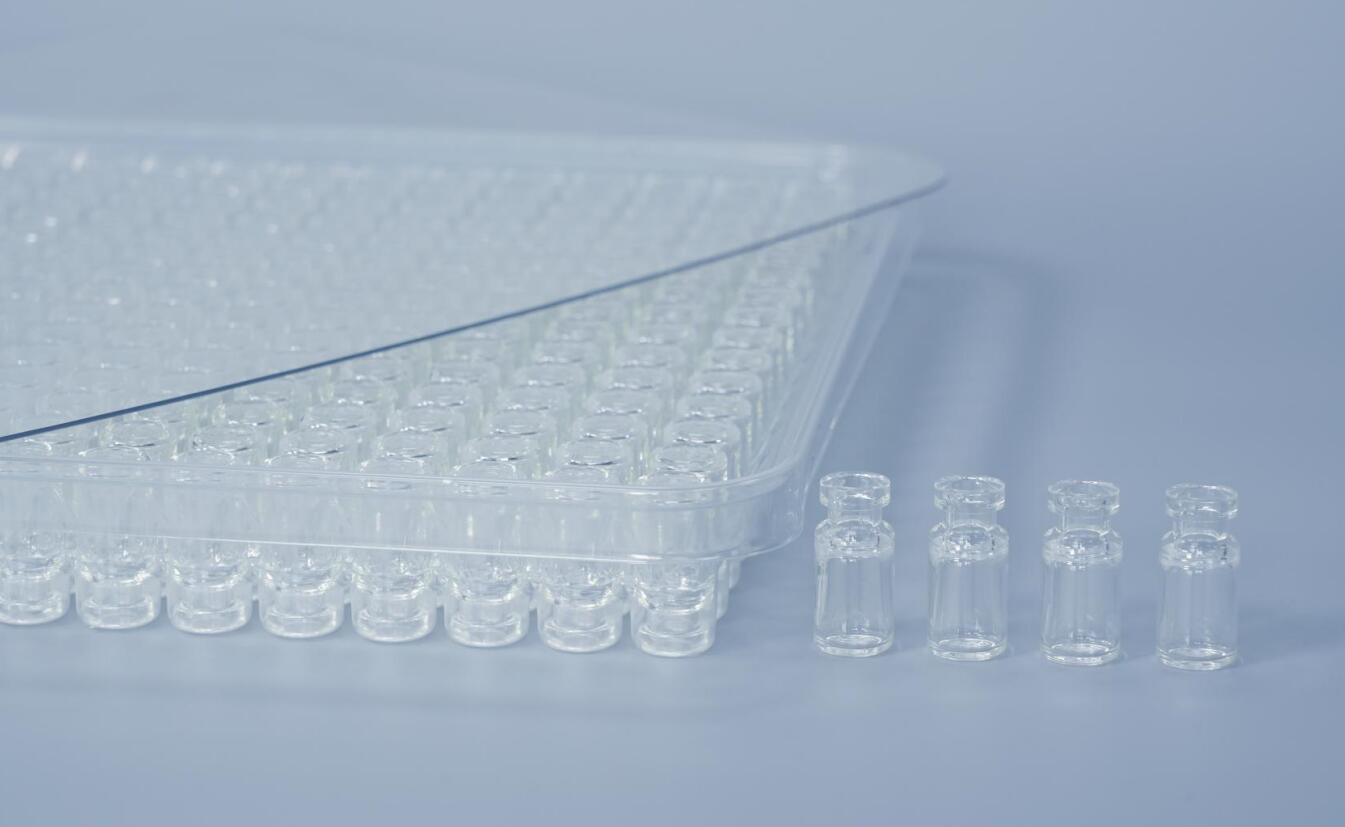
为确基因修饰类冻干制剂(如mRNA疫苗、病毒载体)在COP西林瓶中的极端温度稳定性,需设计多维度密封性验证实验,核心围绕容器密封完整性(CCI) 在深低温下的维持能力。以下为基于法规与技术的实验设计要点:
COP西林瓶
一、实验设计原则
法规依据
遵循USP<1207>、EudraLex Annex 1及日本药典对CCI的要求,覆盖从-80℃(超低温冰箱)至-196℃(液氮)的存储场景。
满足基因治疗产品对无菌性和活性保留的严苛标准(如EMA对AAV载体泄漏率≤10⁻⁶ mbar·L/s的要求)。
材料特性适配
COP的低热膨胀系数(7.0×10⁻⁵/℃)与胶塞(溴丁基橡胶)匹配,避免温度骤变导致密封失效。
利用COP的低温抗裂性(断裂强度达64.3 MPa,为玻璃瓶的5-10倍)抵抗冻融应力。
二、核心验证方法
1. 氦质谱检漏法(高精度定量)
步骤:
将COP西林瓶抽真空后注入氦气(示踪气体),置于液氮(-196℃)中模拟极端存储。
使用氦质谱仪扫描瓶体与胶塞接口,检测泄漏率(目标≤1×10⁻⁸ mbar·L/s)。
优势:可检出0.1 μm级微漏,灵敏度高于传统方法10³倍。
2. 真空衰减法(无损定性)
步骤:
将样品放入真空腔,抽真空至5 mbar,监测压力回升速率(液氮存储后测试)。
压力变化>0.5 mbar/min判定为泄漏(依据ASTM F2338)。
适用场景:冻干粉灌装后的在线快速检测。
3. 染料渗透测试(可视化验证)
步骤:
将COP西林瓶浸入荧光染料(如0.1%亚甲基蓝溶液),施加-0.8 bar负压,液氮冷冻24小时。
解冻后紫外灯检查瓶内染料渗透(阴性为通过)。
案例:AT-Closed Vial®技术通过-196℃/15个月染料测试,泄漏率为0%。
三、极端温度模拟策略
1. 深低温循环测试
| 循环条件 | 测试参数 | 检测方法 |
| -80℃↔25℃ | 300次循环,每次4小时 | 氦检漏(每50次) |
| -196℃↔-40℃ | 50次急冷/复温(液氮→超低温冰箱) | 真空衰减+染料渗透 |
2. 长期稳定性验证
存储条件:
-80℃(6个月)、-196℃(12个月),定期取样。
检测指标:
CCI:氦泄漏率、真空维持能力。
产品活性:mRNA完整性(电泳)、病毒载体滴度(TCID₅₀)
四、关键验证指标与标准
| 检测项目 | 合格标准 | 依据 |
| 氦泄漏率 | ≤1×10⁻⁸ mbar·L/s (-196℃) | USP<1207> Class 1 |
| 氧含量变 | Δ≤0.5%(LHA法,液氮存储后) | PDA TR27 |
| 冻干粉吸湿 | ≤1%(18个月,-80℃) | ICH Q1A |
| 微生物侵入 | 0 CFU(枯草芽孢杆菌挑战) | ASTM F1608 |
五、质量控制体系
过程分析技术(PAT)
激光焊接后实时监测密封面微裂纹(光学相干断层扫描)。
质量源于设计(QbD)
设计空间覆盖胶塞压缩率(15-25%)、激光功率(30-50W)等参数,确保低温密封鲁棒性。
运输模拟验证
ISTA 3A标准模拟液氮运输振动,验证后泄漏率变化≤5%。
实施建议
分阶段验证:
研发阶段:氦检漏+染料渗透(覆盖-196℃至40℃梯度);
GMP生产:真空衰减法100%在线检测+冻融循环抽检。
设备选型:
选用集成液氮槽的氦质谱仪(如Leybold Phoenix L300)及自动化真空衰减测试仪。
数据管理:
建立数字孪生模型,预测不同配方冻干粉(如LNP-mRNA)的长期CCI风险。
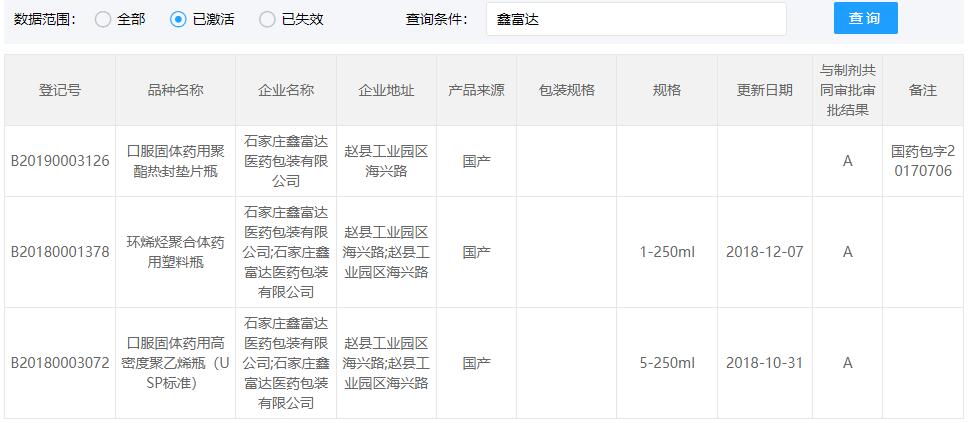
COP西林瓶CDE登记号为A状态
基因修饰类冻干制剂的COP西林瓶密封验证,需以 “材料-工艺-极端环境”三元协同为核心:
材料端:利用COP与胶塞的热膨胀匹配性(Δα<0.5×10⁻⁵/℃)抵御相变应力;
工艺端:激光焊接+伽马辐照键合提升低温密封强度;
验证端:通过氦检漏定量微漏、染料渗透定性定位、真空衰减在线监控,构建三重保障体系。唯有将深低温验证嵌入产品全生命周期,方能突破-196℃稳定性瓶颈,为基因治疗提供合规可靠的活性载体容器
 咨询热线:400-888-1942
咨询热线:400-888-1942