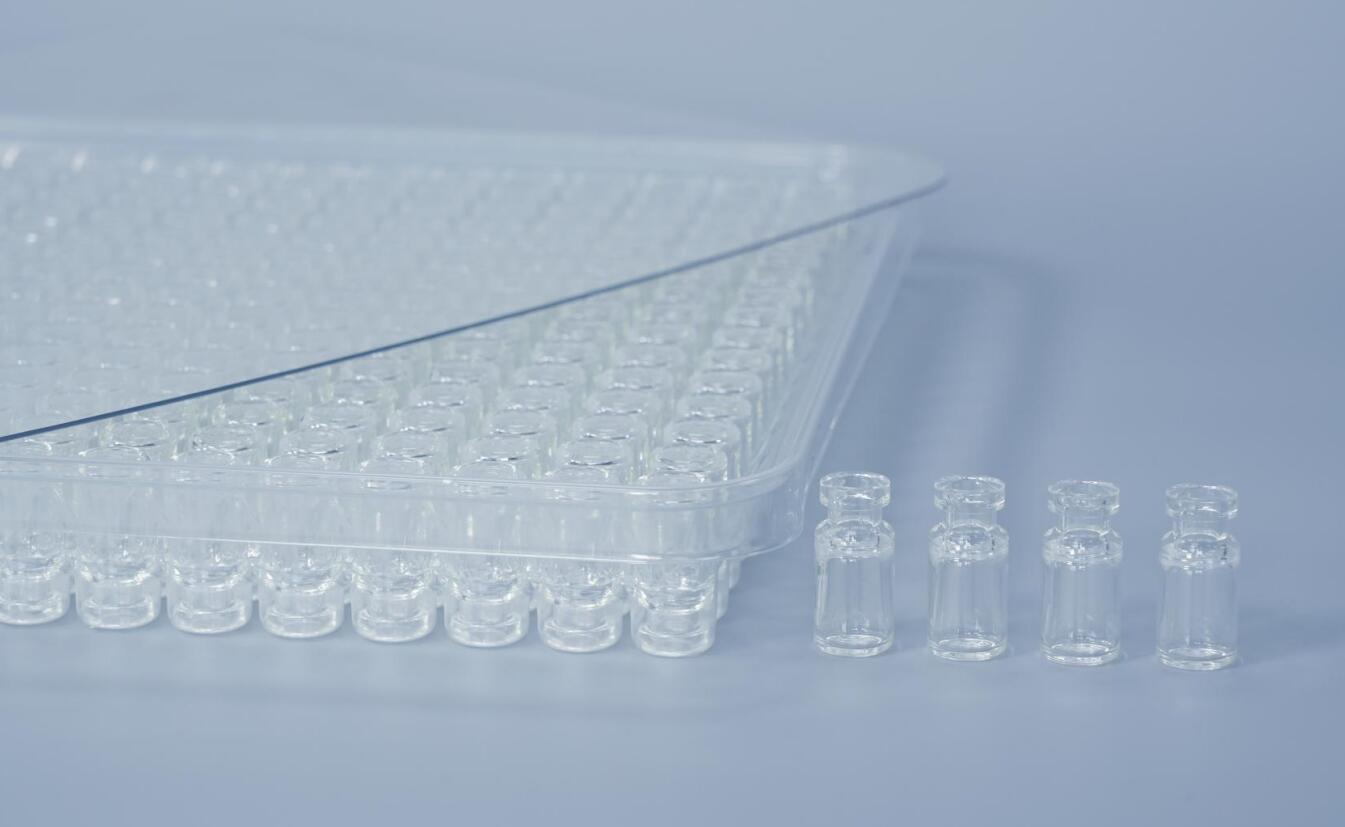
COP西林瓶因其材料特性,在CAR-T细胞治疗这类对包装系统要求极高的领域,其验证工作严谨且深入。下面这个表格汇总了核心的验证维度与方法,可以帮助你快速把握要点。
| 验证维度 | 关键性能指标 | 主要验证方法 | 典型数据/效果 (针对CAR-T等细胞基因药物) |
| 物理稳定性与密封性 | 极低温耐受性、抗压强度、密封完整性 | 液氮浸没法、氦质谱检漏、冻融循环试验、模拟运输振动试验 | -196℃液氮存储下,体积变化率≤0.02%;氦泄漏率≤1×10⁻⁸ mbar·L/s;300次冻融循环后无开瓶力衰减 |
| 化学相容性 | 低蛋白吸附、化学惰性、可提取物/浸出物 | 蛋白吸附测试、GC-MS分析、细胞毒性试验(如ISO 10993-5) | 蛋白吸附量显著低于传统材料;细胞活性≥90%;游离单体释放量≤0.1 ppm |
| 功能性适配验证 | 工艺适配性(如灌装、压塞、轧盖)、标识清晰度 | 模拟灌装试验、自动化生产线运行测试、激光打码读取率测试 | 薄壁强化设计(壁厚0.8-1.2mm)抗压强度达15MPa(-80℃);内壁激光打码在-196℃下读取率≥99.9% |
| 法规符合性 | 符合《中国药典》、USP <661.1>、FDA 21 CFR等 | 第三方检测、供应商审计、材料准入测试、微生物挑战试验 | 通过PDA TR27对细胞治疗制品包装完整性的要求;溶出物检测涵盖17项基因毒性杂质 |
基于以上验证数据,在选择和使用COP西林瓶用于CAR-T细胞治疗时,建议你重点关注以下几点:
关注全流程质量协议:与供应商确认其产品是否具备完整的可提取物和浸出物(E&L)研究报告、细胞毒性测试报告以及密封完整性验证报告。这些是确保包装系统安全性的基石 。

COP西林瓶
进行工艺参数优化:COP材料的弹性模量与玻璃不同,因此在转入自动化生产线时,可能需要微调压塞机的压力参数和轧盖机的扭力设置,以确保密封系统的稳定性和一致性 。
确认法规登记状态:在中国市场,务必确认所使用的COP西林瓶已在CDE获得 “A”状态登记,这代表了原辅包登记资料的完整性已通过形式审查 。
COP西林瓶通过系统化的严格验证,在物理稳定性、化学相容性和生产功能性方面展现出显著优势,能够满足CAR-T细胞治疗药物在超低温储存、保持活性和保证剂量准确性方面的苛刻要求。
 咨询热线:400-888-1942
咨询热线:400-888-1942