基因治疗产品(如AAV、LV病毒载体、CAR-T细胞等)的商业化成功,高度依赖于其在深低温(-80°C至-196°C)下长期储存及复苏后的活性与功能完整性。作为产品的最终“栖息地”,初级包装的选择直接决定了冻存环节的成败。传统硼硅玻璃瓶曾长期占据主导地位,但其在极端低温下的物理与化学局限性日益凸显。相比之下,环烯烃聚合物(COP)西林瓶凭借其材料学的革新,正成为保障基因治疗产品“冻存-复苏”全周期稳定性的更优解。本文将通过关键性能指标的对比,揭示COP西林瓶如何重塑基因治疗产品的低温储存标准。
COP西林瓶
一、 核心挑战:基因治疗产品冻存复苏对包装的严苛要求
基因治疗活性成分对温度波动、机械应力、界面相互作用极为敏感。冻存复苏过程的核心挑战包括:
物理完整性风险:急速降温与复温产生的热应力可能导致容器破裂或产生微裂纹,造成产品泄漏、污染甚至完全失效。
低温密封失效:容器与胶塞因材料热膨胀系数差异,在深低温下收缩不同步,产生微间隙,导致液氮渗入或样品水分升华。
活性成分损失:病毒衣壳蛋白、细胞膜表面蛋白或核酸等生物大分子在容器内壁的非特异性吸附,导致检测滴度失真和实际给药剂量不足。
冰晶损伤:不均匀的冷却会在容器内壁不规则处引发大冰晶成核,刺穿细胞膜或破坏病毒衣壳结构。
二、 性能对决:COP西林瓶 vs. 玻璃瓶的关键数据对比
以下从多个维度对比两种材料在基因治疗冻存场景下的表现:
| 性能维度 | COP西林瓶 | 传统玻璃西林瓶 | 对基因治疗产品的核心影响 |
| 低温抗裂性与机械强度 | 断裂强度是传统玻璃瓶的5-10倍;10次冻融循环后破裂率为0% | 存在冷爆风险,尤其在液氮(-196°C)环境下;内部研究显示破裂风险≥5% | 保障物理完整性:杜绝因瓶体破裂导致的整批珍贵药物报废和交叉污染风险,为价值数百万的细胞治疗产品提供安全屏障 |
| 低温尺寸稳定性与密封性 | 热膨胀系数(60-70×10⁻⁶/℃)与溴丁基胶塞(190220×10⁻⁶/℃)匹配度更佳;-196°C下体积变化率≤0.02% | 热膨胀系数与胶塞差异显著(玻璃约3-5×10⁻⁶/℃),低温下易因收缩不同步产生微间隙 | 维持容器密封完整性:防止液氮渗入污染或样品水分流失,确保长期储存的绝对无菌环境。氦泄漏率可稳定在≤1×10⁻⁶ mbar·L/s |
| 蛋白/核酸低吸附性 | 表面蛋白吸附率≤0.05 μg/cm²;对DNA吸附回收率损失可控制在<5% | 蛋白吸附率>0.3 μg/cm²;病毒颗粒易吸附于玻璃表面导致滴度损失 | 确保剂量准确性与分析可靠性:最大限度减少病毒载体、外泌体等活性成分的损失,使QC检测值更真实,避免因吸附导致的剂量失真和疗效波动。 |
| 深低温下细胞/病毒存活率 | CAR-T细胞(-196°C/6个月):活率95.20%;AAV载体(-80°C/24个月):活性保留96.5% | CAR-T细胞(-196°C/6个月):活率83.50%;AAV载体(-80°C/24个月):活性保留88.2% | 直接提升产品效价与疗效:更高的复苏后活性和病毒基因组完整性,直接转化为更可靠的治疗效果和更高的商业化成功率。 |
| 化学惰性与相容性 | 极高的化学纯度,游离单体释放量极低(≤0.1 ppm);耐受DMSO等冻存保护剂,无有害浸出物 | 可能存在碱性离子析出风险,与敏感制剂发生相互作用的概率更高。 | 保障产品纯度与安全性:为敏感的基因治疗产品提供惰性环境,避免因包装材料引入的杂质影响产品稳定性和引发不必要的免疫反应。 |
三、 机理探析:COP材料为何更胜任深低温环境?
本征材料优势:COP由饱和碳氢链构成,结构对称且无定形,使其在从室温到-196°C的广阔温区内能保持优异的尺寸稳定性和柔韧性,无玻璃化转变导致的脆性突变点。
热力学匹配设计:COP与常用药用胶塞的热膨胀系数更为接近,确保在温度剧变时,整个密封系统协同收缩/膨胀,从根本上杜绝了因应力集中导致的泄漏。
表面工程学:通过等离子体处理等技术,COP内壁可形成光滑、均一且低表面能的界面,不仅减少生物大分子吸附,还能促进溶液均匀成核,形成细小且均匀的冰晶,最小化对细胞和病毒颗粒的机械损伤。
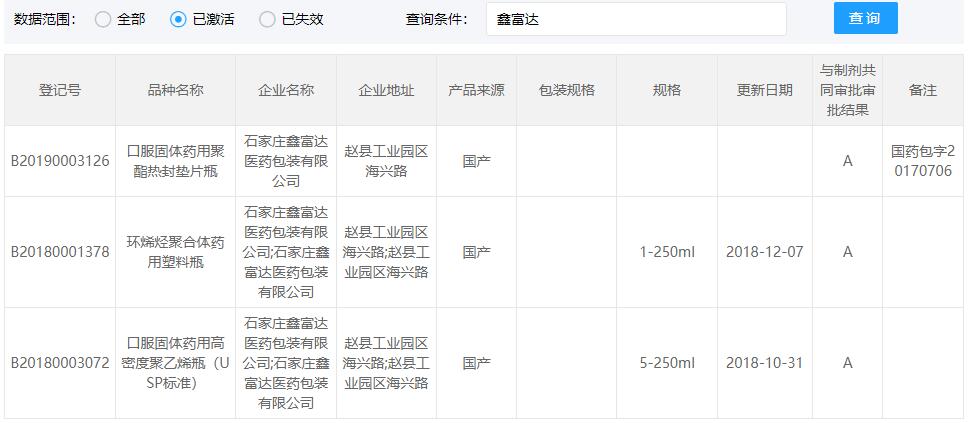
COP西林瓶CDE登记号为A状态
四、 结论:为基因治疗的“低温长征”选择确定性
冻存不是终点,而是确保基因治疗产品能够安全、有效抵达患者体内的关键中转站。面对-80°C乃至-196°C的极端考验,包装材料的性能直接决定了这场“低温长征”的成败。
综合对比表明,COP西林瓶在机械强度、密封可靠性、低吸附特性以及最终的产品活性保留率方面,均显著优于传统玻璃瓶。它通过材料级的创新,系统性地解决了深低温储存中的物理风险与化学风险,为AAV、LV、CAR-T等高端生物制剂提供了从生产线下游到临床床边的全链条稳定保障。
 咨询热线:400-888-1942
咨询热线:400-888-1942