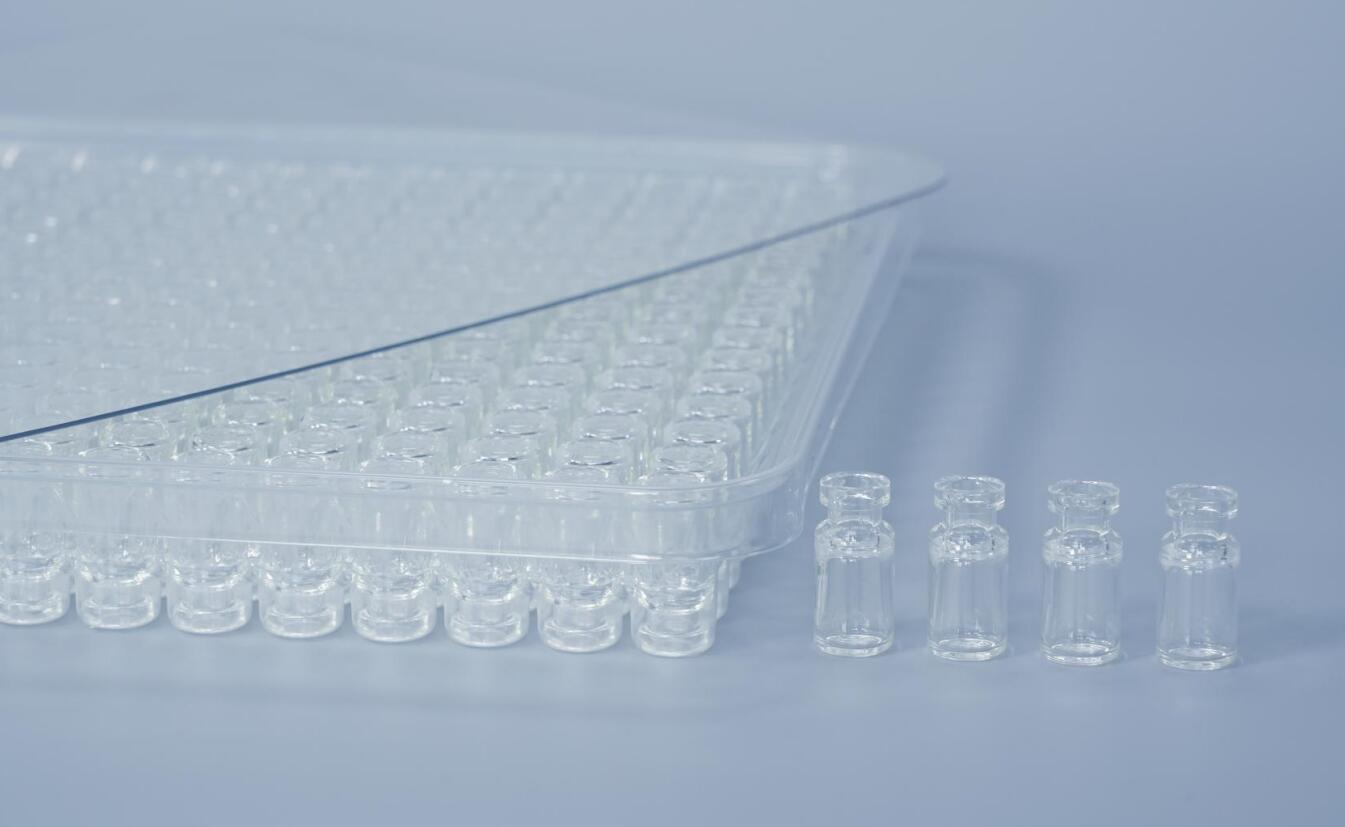
在生物制药与细胞治疗领域,无菌保证是产品质量不可逾越的生命线。传统的西林瓶无菌处理流程,依赖于一套复杂且资源密集的“厂内清洗、灭菌”体系,而随之而来的“清洗验证”更是压在质量与生产部门肩上的重担。如今,采用预辐照灭菌的即用型(RTU)COP西林瓶,正在引领一场无菌保证方案的范式转移,让企业得以彻底告别繁琐的清洗验证,拥抱更简化、更可靠、更高效的无菌控制策略。
COP西林瓶
一、 传统清洗验证:一个昂贵、复杂且持续的风险点
对于使用传统玻璃西林瓶的生产线,为确保无菌,必须建立并维护一套完整的厂内处理流程:
清洗:去除微粒、内毒素。
硅化(如需要):防止蛋白或细胞吸附。
高温灭菌/除热原:通常采用250°C以上的干热灭菌。
清洗验证:这是核心挑战。它并非一次性工作,而是一个持续的、周期性的质量活动,要求企业证明:
清洗效果:能持续将污染物(微粒、内毒素、清洁剂残留)降至可接受标准以下。
灭菌效果:干热灭菌柜的热分布、热穿透均一性,以及其对内毒素的破坏能力(通常要求3个对数下降值)。
硅化均匀性:硅油涂布的均一性与残留量可控。
设备与程序:任何变更(如清洗水温度、灭菌时间、设备部件更换)都可能触发再验证。
这个过程消耗数百至数千工时,占用昂贵的生产设备进行验证批次,产生海量文件,并持续面临因验证失败或监管质疑而导致的生产中断风险。
二、 辐照灭菌:一种经过验证的、终端化的无菌保证方法
γ射线或电子束(E-beam)辐照灭菌是一种成熟的、终端化的灭菌方法。对于COP西林瓶,其简化无菌保证的逻辑在于:
原理可靠:高能射线直接破坏微生物的DNA或RNA,使其失去复制能力,达到无菌要求。
参数放行:灭菌效果由精确控制的辐照剂量(通常为25-40 kGy)决定,该剂量经过严格的微生物挑战试验(如使用短小芽孢杆菌孢子)验证,确保达到10^-6的无菌保证水平(SAL)。过程依赖于物理参数(剂量)的监控,而非对最终产品的破坏性取样。
供应商转移:辐照灭菌及相关的验证工作(包括剂量分布研究、生物负载监测、材料相容性测试)由COP西林瓶供应商在专业辐照中心完成,并形成完整的验证主文件(如辐照验证报告)。
RTU免洗免灭COP西林瓶
三、 COP西林瓶与辐照灭菌的协同优势:如何实现“简化”?
COP材料与辐照灭菌技术的结合,创造了独特的简化优势:
材料耐受性极佳:COP(环烯烃聚合物)具有优异的耐辐照性能。在有效灭菌剂量下,其物理性能(透明度、机械强度)和化学性能(低浸出物)保持稳定,不会像某些塑料那样发生黄变或脆化,这是实现“即用型”的前提。
“无菌状态”的转移:COP西林瓶在洁净环境下生产后,立即进行密封包装,然后整体进行辐照灭菌。这意味着,无菌性是在最终密封的初级包装上实现的。企业接收到的每一支西林瓶,都是一个已被验证的、独立的“无菌单元”,无需担心在拆包、上料前的环节被污染。
彻底消除厂内清洗验证:这是最根本的简化。企业不再需要:
验证清洗机对不同污染物的清除能力。
验证干热灭菌柜的除热原效力。
验证硅化工艺的均一性。
进行持续的清洗水、内毒素等监测。
应对因清洗验证带来的监管审计问询。
质量部门的职责从“执行和证明复杂的厂内过程”转变为“审核和确认供应商提供的成熟验证包”,工作量与风险呈数量级下降。
简化微生物控制策略:企业的微生物控制重点可以更聚焦于核心工艺环节——如无菌灌装操作(A级区环境)、人员培训、培养基模拟灌装验证,而非分散精力于上游的包装清洗灭菌环节。这使无菌保证体系更加清晰和专注。
四、合规性更清晰:基于供应商责任的监管认可
全球主要药监机构(如FDA、EMA、NMPA)均认可经充分验证的辐照灭菌作为终端灭菌方法。其合规路径更清晰:
主文件支持:领先的COP西林瓶供应商会准备详细的药物主文件(DMF)/ 活性物质主文件(ASMF),其中包含完整的辐照灭菌验证资料、材料表征和稳定性数据,供药企引用至其上市申请中。
审计重点转移:监管审计的重点从审计企业的清洗灭菌车间,转向审计COP西林瓶供应商的质量体系和辐照服务提供商的资质与控制。选择拥有强大质量体系和可靠供应链的供应商,本身就是一种风险外包和合规强化。
变更管理简化:当供应商的辐照工艺经过验证并备案后,其生产的多批次产品具有高度一致性。企业无需担心厂内灭菌柜性能波动带来的批次间差异。
五、超越简化:带来的额外效益
降低交叉污染风险:完全避免了共线生产时,因清洗不彻底导致的交叉污染风险,特别适合多产品生产的CDMO或拥有复杂产品管线的企业。
提升生产灵活性:生产线可以快速切换不同产品,无需等待漫长的清洗线清洁验证。
节约资源与成本:节省验证成本、设备投资(清洗机、灭菌柜)、能耗(干热灭菌耗能巨大)及相关的实验室检测费用。
加速上市进程:对于新建生产线,可以省去长达数月的清洗验证周期,加速工艺验证和商业化生产启动。
结论:迈向更智能的无菌保证未来
“告别清洗验证”并非降低标准,而是通过技术创新和专业化分工,将无菌保证建立在更科学、更可控、更高效的基石之上。采用预辐照灭菌的COP西林瓶,将复杂的灭菌工艺及其验证责任,转移给拥有专业设备和知识的供应商,使制药企业能够集中核心资源于药物本身的生产与研发。
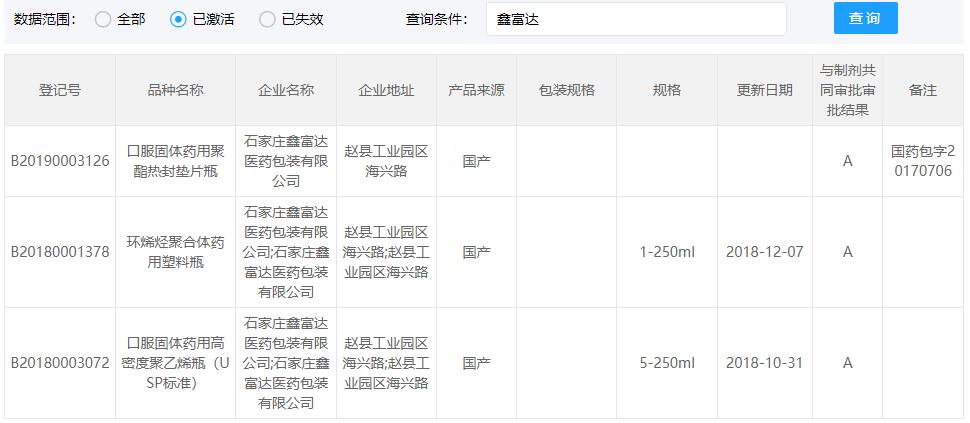
COP西林瓶CDE登记号为A状态
对于正在构建或优化无菌生产体系的企业而言,这代表了一种更智能的风险管理策略和运营效率提升路径。我们建议,在下一代生物药或细胞治疗产品的工艺设计之初,就将即用型预灭菌COP西林瓶作为默认选项进行评估。这不仅是为了简化今天的工作,更是为了构建面向未来的、更具韧性与竞争力的生产体系。
 咨询热线:400-888-1942
咨询热线:400-888-1942