儿童安全盖(Child-Resistant Closure, CRC盖)对于氨溴特罗、氨溴索等儿科常用口服溶液而言,更多被视为一项“加分项”或“推荐配置”。然而,随着国家药品监管体系的全面升级与对儿童用药安全底线的坚决捍卫,这一局面已发生根本性逆转。今天,符合国家强制标准的儿童安全盖,已不再是包装设计的“可选项”,而是决定产品能否成功注册上市、能否持续合规销售的“必选项”与“关键项”。
一、法规的“分水岭”:2025版药典与GB/T 25163-2025的双重驱动
儿童安全盖从“可选”到“必选”的质变,核心驱动力来自于两项具有里程碑意义的法规标准更新,它们共同构成了当前及未来注册申报的刚性门槛。
1.《中国药典》2025版的法定强制力
2025年版《中华人民共和国药典》已于2025年3月25日正式颁布,并于2025年10月1日起强制实施。作为国家药品标准的法定核心,其构建的“1+4+58”药包材标准体系是总纲领。其中,《9624 药品包装用塑料材料和容器指导原则》已明确要求防儿童开启功能需通过认证。这意味着,自2025年10月1日起,所有新提交的药品注册申请,其申报资料中关于包装系统的研究数据必须完全符合新药典要求,儿童安全性能成为关联审评的必备内容。
2. GB/T 25163-2025国家标准的全面接轨
新版国家标准《防止儿童开启包装可重新盖紧包装的要求与试验方法》(GB/T 25163-2025)已于2025年6月30日发布,并于2026年1月1日起强制实施。该标准修改采用了国际标准ISO 8317:2015,其核心要求是:在无演示的5分钟内,至少85%的42-51月龄儿童无法开启;演示后,整个10分钟内至少80%的儿童无法开启;同时,90%的50-70岁成人能在5分钟内开启并重新盖紧。这为儿童安全盖的性能提供了量化的、与国际接轨的测试标杆。
口服液体药用高密度聚乙烯瓶60ml儿童安全盖
二、对注册申报工作的直接影响:三大关键转变
法规的升级直接重塑了氨溴特罗、氨溴索等口服溶液从研发到申报的全流程。
1. 关联审评中的“一票否决”风险
根据《药品注册管理办法》,我国对直接接触药品的包装材料和容器实行关联审评审批制度。如今,儿童安全盖作为包装系统的核心部件,其合规性直接关联制剂产品的审评结果。如果申报资料中无法提供符合GB/T 25163-2025标准的儿童安全盖验证报告,或相容性研究不充分,很可能导致整个注册申请被要求补充资料甚至不予批准。儿童安全盖已从包装附件,跃升为与API、辅料同等重要的关键原辅包。
2. 申报资料要求的深度与广度扩展
儿童防护性能测试报告:必须提供由具备资质的第三方实验室出具的、证明其完全符合GB/T 25163-2025标准的正式测试报告。
全面的相容性研究:2025版药典对相容性研究提出了更细致的要求。对于氨溴特罗、氨溴索等具体品种,需重点关注包装材料(尤其是盖内垫片)对活性成分、防腐剂的吸附性,以及材料中可提取物向药液中的迁移风险。
功能性与稳定性关联数据:需提供儿童安全盖在加速及长期稳定性考察条件下的密封性能(如负压密封测试)、开启扭矩及其衰减率数据,证明其在产品有效期内性能始终可靠。
3. 明确且紧迫的时间表
2025年10月1日:此后所有新提交的注册申请,必须符合2025版药典要求。
2026年1月1日:所有生产上市的适用药品,其儿童安全性能必须符合GB/T 25163-2025。
2026年4月1日:对于此前已上市的产品,过渡期结束,必须完成包装变更以符合新规。
三、针对氨溴特罗、氨溴索等品种的特殊考量
对于这类粘稠、糖浆状的口服溶液,儿童安全盖的选型与验证需格外注意:
防粘附与密封持久性:糖浆易在瓶口残留,干燥后可能结晶,影响盖子的重复密封性。应选择具有抗粘附涂层的垫片,并在稳定性研究中重点关注多次开启后的密封性能。
化学相容性:需验证垫片材料(如硅胶)对处方中特定成分(如矫味剂、防腐剂)无吸附,确保产品化学稳定性。
使用便利性:考虑到患儿需每日多次服药,盖子的设计必须在确保儿童安全的前提下,为家长(尤其是老年人)提供足够的便利性,符合“成人易用”的强制要求。
口服液体药用聚丙烯瓶20ml
四、企业的战略应对:从被动合规到主动赋能
1. 研发前端介入,实现“设计即合规”
在制剂研发初期,就将符合最新标准的儿童安全盖作为关键设计输入。与专业的包材供应商合作,提前进行包材筛选、相容性预研究和儿童安全测试,避免在注册申报后期因包装问题导致重大延误。
2. 构建完整、模块化的注册证据包
系统性地生成并整理以下模块化资料,为高效申报奠定基础:
包材登记信息(A状态登记号)。
符合GB/T 25163-2025的儿童安全测试报告。
详尽的包材相容性研究(可提取物/浸出物)报告。
包材功能性与药品稳定性的关联研究数据。
3. 区分在研新品与已上市产品的合规路径
在研及新报产品:必须直接按照2025版药典和GB/T 25163-2025的最高标准进行全套研究并申报。
已上市产品:需立即启动包装系统变更研究,按照《药品上市后变更管理办法》的要求,评估变更等级(通常为中等变更),开展对比研究与稳定性考察,并在2026年4月1日前完成备案或补充申请。
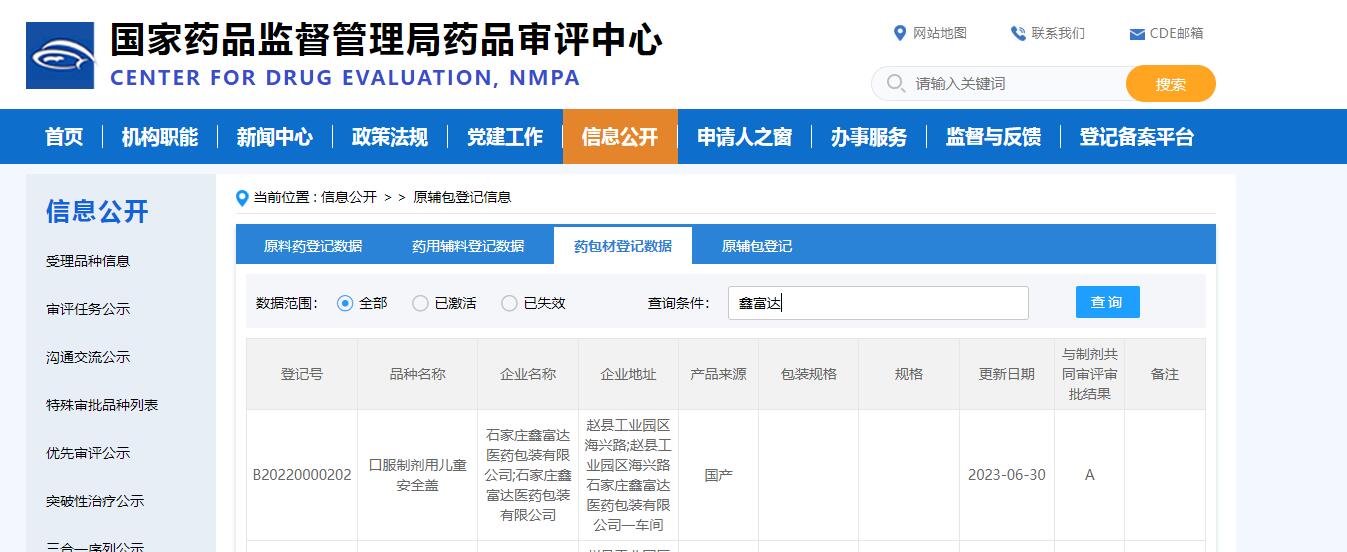
口服液体药用聚丙烯压旋盖CDE登记号为A状态
结语
儿童安全盖在氨溴特罗、氨溴索等口服溶液注册申报中从“可选”到“必选”的地位变迁,是国家守护儿童用药安全决心的最直接体现。这不仅是法规条文的更新,更是整个行业对产品质量与患者安全责任认知的集体升华。
对于制药企业而言,顺应这一趋势,绝非被动满足监管要求,而是主动构建产品核心竞争力的战略机遇。一个经过严谨验证、性能卓越的儿童安全盖,是产品说明书上无声的“安全承诺”,是传递给患儿家长最重要的“信任基石”,也是在同质化市场中脱颖而出的“品牌宣言”。在儿童用药安全这座不容有失的丰碑前,选择合规、可靠的儿童安全盖,已是我们共同且必须履行的责任。让我们以最高的标准,为每一滴药液,扣上最牢固的“安全锁”。
 咨询热线:400-888-1942
咨询热线:400-888-1942







