氨溴索口服溶液作为儿科呼吸系统疾病的一线用药,其质量稳定性直接关系到患儿的治疗效果与用药安全。在药品的整个生命周期中,有效期的确定是研发与注册的核心。然而,一个常被低估的关键因素正日益凸显:儿童安全盖(CRC盖)的密封性能。它并非一个被动的包装组件,而是动态影响药物化学、物理及微生物稳定性的“活性界面”。本文将深入剖析,口服液体药用聚丙烯压旋盖的密封性能如何成为决定氨溴索口服溶液有效期的“隐形守门人”。
口服液体药用聚丙烯压旋盖
一、密封失效:通往药物降解的“三道门”
一个理想的密封系统,应在有效期内持续提供对氧气、水汽、微生物和污染物的屏障。儿童安全盖密封性能的衰减,会依次打开三道影响稳定性的“大门”:
1. 第一道门:水蒸气透过——引发水解与物理变化
氨溴索本身具有一定的引湿性。如果盖子的密封性能不足,环境中的水蒸气会持续渗入包装内部。
化学影响:可能加速氨溴索活性成分的水解反应,导致有关物质(降解产物)含量超标,药效降低。
物理影响:导致溶液密度、粘度发生改变,可能影响给药剂量的准确性。糖浆类制剂还可能出现结晶、沉淀或霉变。
微生物影响:为微生物生长提供了必要的水分条件。
2. 第二道门:氧气渗入——催化氧化反应
氧气是许多药物降解反应的催化剂。密封不严会导致包装顶空氧气浓度随时间升高。
对氨溴索的影响:可能诱发氧化降解途径,生成新的氧化杂质,不仅影响含量,更可能引入未知安全风险的降解产物。
对辅料的影响:处方中的矫味剂、防腐剂(如尼泊金酯类)也可能被氧化,导致口味改变或防腐效力下降。
3. 第三道门:微生物侵入——直接的安全威胁
口服液体制剂并非无菌产品,但必须符合《中国药典》的微生物限度标准。密封性能下降,特别是在多次开启后,意味着微生物屏障失效。
风险:环境中的细菌、霉菌可能侵入,导致微生物限度检查不合格。对于不含强效防腐剂的处方,风险更高。
二、儿童安全盖密封性能的“三重衰减”机制
在长达数年(如24个月)的有效期内,儿童安全盖的密封性能并非恒定,其衰减主要受三大机制驱动:
1. 材料应力松弛与蠕变
盖内的弹性体密封垫片(常用硅胶)在持续受压状态下,会发生应力松弛(密封力随时间下降)和蠕变(材料发生缓慢的塑性变形)。这会导致垫片对瓶口的回弹力减弱,密封压力降低,水汽和氧气透过率(WVTR/OTR)随之升高。高温高湿的储存环境(如夏季家庭药箱)会显著加速这一过程。
2. 多次开启的疲劳效应
氨溴索口服溶液作为多剂量包装,在整个使用周期内会被反复开启数十次。每次开启和再关闭,都是一次对密封系统的机械疲劳:
垫片压缩永久变形:材料在反复压缩后无法完全恢复原状。
螺纹磨损:瓶盖与瓶口的塑料螺纹轻微磨损,导致达到相同密封效果所需的扭矩发生变化。
药液残留干扰:粘稠的溶液在瓶口残留,干燥后可能形成结晶,破坏密封面的平整接触。
3. 化学相容性导致的材料劣化
氨溴索口服溶液的特定处方(pH值、溶剂、防腐剂)可能与密封垫片材料发生相互作用。
可提取物与浸出物:垫片中的低分子量物质可能迁移至药液中,成为新的杂质。
材料溶胀或硬化:药液中的成分可能导致垫片材料发生溶胀(影响密封力)或硬化脆化(失去弹性),从而破坏密封。
口服液体药用高密度聚乙烯瓶60ml压旋盖
三、科学评估:将密封性能纳入稳定性研究方案
传统的稳定性研究主要关注药物本身,现代研究要求必须将包装系统性能作为关键变量进行关联考察。
1. 密封完整性的定量监测
在长期和加速稳定性试验中,不应仅凭“目视检查”判断密封。应定期(如0、3、6、12、18、24个月)抽样,使用确定性方法进行密封完整性测试:
真空衰减法:这是目前检测口服液体制剂包装微量泄漏最灵敏、最客观的方法之一。通过监测测试腔内的压力变化,可以量化包装的泄漏率,建立其随时间变化的曲线,为有效期预测提供数据支持。
2. 关键质量属性的关联分析
在稳定性考察点,除了检测氨溴索的含量、有关物质、pH值、微生物限度等,还应同步检测:
包装顶空氧含量:使用顶空分析仪,直接监测瓶内氧气浓度是否随时间异常升高,这是密封失效的直接证据。
水蒸气透过量:可通过称量整个包装在稳定性条件下的重量变化来间接评估。
开启/再密封扭矩:测量并记录每次抽样时瓶盖的扭矩值,追踪其衰减趋势。
3. 模拟使用后的稳定性挑战
在稳定性方案中增设“模拟使用”组。样品在初始稳定性考察点(如6个月)被定期开启/关闭一定次数(模拟实际用药),然后继续放回稳定性条件考察。将此组数据与“始终未开启”的对照组进行比较,能直接揭示多次使用对密封性能及药品稳定性的真实影响。

口服液体药用聚丙烯瓶100ml
四、基于密封性能的有效期确定与延展策略
密封性能数据直接影响有效期的设定,并为企业提供优化空间。
1. 有效期的“短板”原则
药品的有效期由稳定性研究中最先不符合标准的项目决定。如果因为密封性能衰减,导致在第18个月时有关物质超标或微生物超标,那么即使主成分含量仍合格,有效期也只能定为18个月。因此,提升密封可靠性就是直接延长有效期的潜在途径。
2. 策略:选择与验证高可靠性密封系统
材料科学:选择具有低压缩永久变形率、低透气性的高性能密封材料(如特种硅胶或热塑性弹性体)。
结构设计:采用双道密封(如顶面密封+侧面密封)或锥面密封设计,其对制造公差和材料疲劳的容忍度更高。
工艺控制:确保生产线上旋盖机的扭矩控制极其精准和稳定,为整个有效期的密封性能提供一致的初始保障。
加速预测:利用密封材料在高温下的老化数据,结合稳定性研究结果,建立模型,更科学地预测长期密封性能。
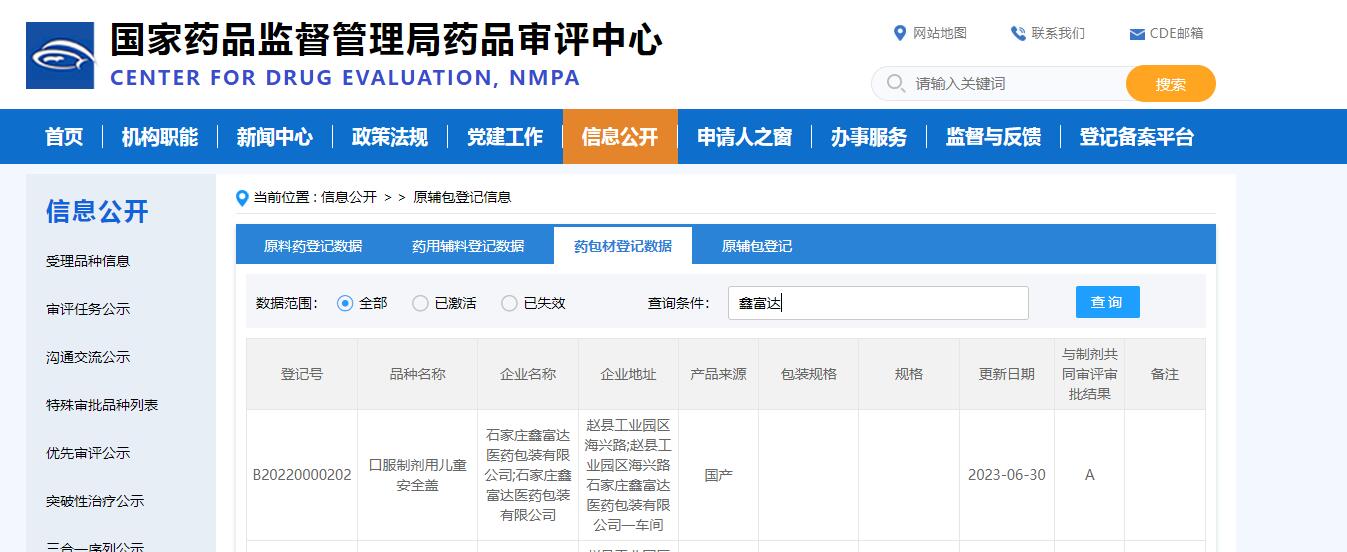
口服液体药用聚丙烯瓶压旋盖CDE登记号为A状态
五、符合法规的完整证据链
在药品注册申报时,关于包装系统与稳定性的研究必须形成完整证据链:
包材选择依据:说明所选儿童安全盖的密封原理、材料特性及其与制剂处方的相容性研究结论。
密封性能验证:提供包装密封完整性(如真空衰减法)的方法学验证及初始检测报告。
稳定性关联数据:在稳定性研究报告中,明确展示各考察点密封性能测试(如顶空氧、扭矩)结果及其与药品关键质量属性(CQAs)变化的关联性分析。
有效期论证:基于包含密封性能在内的全部稳定性数据,综合论证所申请有效期的合理性。
结语
对于氨溴索口服溶液而言,儿童安全盖的密封性能绝非一个静态的包装参数,而是一个贯穿药品整个生命周期、动态影响其内在质量的关键质量属性。它如同一道随时间缓慢变化的“防线”,其坚固程度直接决定了药物对抗环境侵蚀的能力,从而最终划定有效期的边界。
在儿童用药安全被置于前所未有高度的今天,制药企业必须超越“盖子能盖紧”的简单认知,从材料科学、机械设计、工艺控制和稳定性研究的深度关联中,重新审视并定义儿童安全盖的密封性能。这不仅是为了满足日益严格的法规合规要求,更是为了兑现对每一位患儿及其家庭的质量承诺——确保在标签注明的有效期内,每一滴药液都安全、有效、纯净如初。
 咨询热线:400-888-1942
咨询热线:400-888-1942






