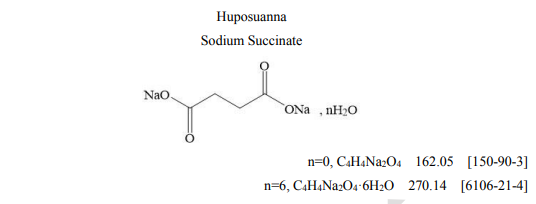
本品为1,4-丁二酸二钠盐无水物或六水合物。按干燥品计算,含琥珀酸钠(C4H4Na2O4)应为 98.0%~102.0%。
【性状】本品为白色结晶或结晶性粉末。
【鉴别】(1)本品显钠盐鉴别的反应(通则 0301)。
(2)在含量测定项下记录的色谱图中,供试品溶液主峰的保留时间应与对照品溶液主峰的保留时间一致。
(3)本品红外光吸收图谱应与对照图谱(附图)一致(通则0402)。
【检查】碱度 取本品1.0g,加水 20 ml溶解后,依法测定(通则 0631),pH值应为7.0~9.0。
硫酸盐 取本品1.0g,依法检查(通则0802),与标准硫酸钾溶液1.9ml 制成的对照液比较,不得更浓(0.019%)。
醋酸钠、马来酸钠和富马酸钠 照高效液相色谱法(通则 0512)测定。
供试品溶液 取本品适量,精密称定,加 1%磷酸溶解并稀释制成每1ml中约含 10 mg的溶液。
醋酸贮备液 取冰醋酸适量,精密称定,加 1%磷酸定量稀释制成每1ml中约含 150 μg醋酸的溶液(相当于每 1 ml 中约含 200 μg 的醋酸钠溶液)。
马来酸贮备液 取马来酸对照品适量,精密称定,加 1%磷酸定量稀释制成每1 ml 中约含73μg马来酸的溶液(相当于每1ml中约含100μg的马来酸钠溶液)。
富马酸贮备液 取富马酸对照品适量,精密称定,加 1%磷酸定量稀释制成每1 ml 中约含73μg富马酸的溶液(相当于每1ml中约含100μg的富马酸钠溶液)。
对照品溶液 分别精密量取醋酸贮备液、马来酸贮备液和富马酸贮备液各1 ml,置10 ml量瓶中,加1%磷酸定量稀释制成每1 ml中约含醋酸15μg、马来酸 7.3 μg和富马酸7.3μg的混合溶液。
系统适用性溶液 取无水琥珀酸钠对照品适量,精密称定,加各对照品贮备液适量,用1%磷酸溶解并定量稀释制成每1 ml中约含琥珀酸钠10 mg、醋酸15μg、马来酸7.3μg与富马酸7.3μg的混合溶液。
色谱条件 见含量测定项下。
系统适用性要求 系统适用性溶液色谱图中,各峰之间的分离度应符合要求,其中琥珀酸峰与富马酸峰之间的分离度应不低于2.0。对照品溶液色谱图中,各杂质峰的拖尾因子应在0.8~2.0之间,醋酸峰高的信噪比应不低于10,醋酸峰面积的相对标准偏差应不大于 5.0%。
精密量取供试品溶液和对照品溶液,分别注入液相色谱仪,记录色谱图。供试品溶液色谱图中,醋酸的峰面积不得大于对照品溶液中醋酸的峰面积(相当于醋酸钠不得过 0.2%),马来酸的峰面积不得大于对照品溶液中马来酸的峰面积(相当于马来酸钠不得过 0.1%),富马酸的峰面积不得大于对照品溶液中富马酸的峰面积(相当于富马酸钠不得过 0.1%)。干燥失重取本品,在120℃干燥2小时,减失重量应为 37.0%~41.0%(六水合物),或不得过 2.0%(无水物)(通则 0831)。
钠 照原子吸收分光光度法(通则0406 第一法)测定。
供试品溶液 取本品约 18 mg(无水物)或 30 mg(六水合物),精密称定,置50 ml量瓶中,加氯化铯溶液(取氯化铯 3.175 g,加水溶解并稀释至 50 ml)1.0 ml,用水溶解并稀释至刻度,摇匀。
对照品溶液 取基准氯化钠0.254 g,精密称定,置10 ml量瓶中,加水溶解并稀释至刻度(相当于每1 ml含钠10 mg),摇匀。分别精密量取上述溶液 0.7 ml、0.8 ml、0.9 ml、1.0ml、1.1 ml、1.2 ml、1.3 ml,置100 ml量瓶中,各加氯化铯溶液2ml,用水分别定量稀释制成每1ml中约含钠70μg、80μg、90μg、100μg、110μg、120μg、130μg的对照品溶液。以火焰为原子化器,在330 nm 的波长处分别测定各对照品溶液和供试品溶液的吸光度。按干燥品计算,含钠(Na)应为27.0%~29.8%。
细菌内毒素(供注射用)取本品,用细菌内毒素检查用水溶解并稀释制成每 1ml 中不大于 37.5 mg 的溶液,依法检查(通则1143),每1mg琥珀酸钠中含内毒素的量应小于标示值。
微生物限度(供注射用)取本品,依法检查(通则1105与通则1106),每1g供试品中需氧菌总数不得过100cfu,霉菌和酵母菌总数不得过100cfu,不得检出大肠埃希菌。
【含量测定】照高效液相色谱法(通则 0512)测定。
供试品溶液 取本品适量,精密称定,加1%磷酸溶解并定量稀释制成每1ml中约含琥珀酸钠3mg的溶液。
对照品溶液 取无水琥珀酸钠对照品适量,精密称定,加1%磷酸溶解并定量稀释制成每1ml中约含琥珀酸钠3mg的溶液。
系统适用性溶液 取无水琥珀酸钠对照品和富马酸对照品适量,精密称定,加 1%磷酸溶解并定量稀释制成每1ml中约含琥珀酸钠3mg和富马酸2.2μg的混合溶液。
色谱条件 用十八烷基硅烷键合硅胶为填充剂(4.6mm×150 mm,3.0μm或效能相当的色谱柱),以0.025 mol/L磷酸二氢钾溶液(用磷酸调节pH至2.3)-甲醇(95:5)为流动相;柱温为 30℃;检测波长为 204 nm;进样体积10μl;流速1.0 ml/min。
系统适用性要求 系统适用性溶液色谱图中,琥珀酸峰与富马酸峰之间的分离度应不低于2.0。对照品溶液色谱图中,琥珀酸峰的拖尾因子应在0.8~2.0之间。对照品溶液峰面积的相对标准偏差应不大于0.5%。
精密量取供试品溶液与对照品溶液,分别注入液相色谱仪,记录色谱图。按外标法以峰面积计算。
【类别】缓冲剂和pH调节剂。
【贮藏】密封保存。
【标示】①本品别名琥珀酸二钠。②应标明本品为无水物或六水合物。③应标明每 1 mg琥珀酸钠中含内毒素的量应小于的标示值。
附:
药用辅料琥珀酸钠红外光吸收对照图谱
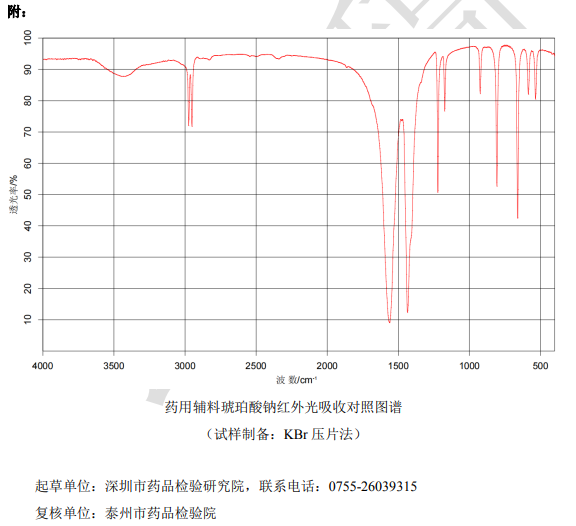
(试样制备:KBr 压片法)
起草单位:深圳市药品检验研究院,联系电话:0755-26039315
复核单位:泰州市药品检验院
琥珀酸钠药用辅料标准草案起草说明
1 命名、含量限度及性状:参考 USP 现行标准和样品实际情况,制订命名、含量限度、性状项。
2 鉴别:参考 USP 现行标准和 ChP 一般鉴别试验(通则 0301),制订钠盐鉴别、液相色谱鉴别和红外鉴别,同时附:药用辅料琥珀酸钠红外光吸收对照图谱(试样制备:KBr 压片法)。
3 检查
3.1 碱度、硫酸盐、干燥失重:依据 USP 现行标准,制订碱度、硫酸盐、干燥失重检查项。
3.2 醋酸钠、马来酸钠和富马酸钠:依据 USP 现行标准,参考含量测定项下的色谱条件,对醋酸钠、马来酸钠和富马酸钠三种杂质进行控制,制订醋酸钠、马来酸钠和富马酸钠检查项。
3.3 钠:琥珀酸钠为 1,4-丁二酸的二钠盐,制订钠检查项,采用原子吸收分光光度法测定钠的含量。
3.4 细菌内毒素(供注射用)、微生物限度(供注射用):供注射用药用辅料琥珀酸钠制订细菌内毒素、微生物限度检查项。
4 含量测定:参考 USP Sodium Succinate 品种含量测定项下的方法,制订高效液相色谱法测定琥珀酸钠的含量。
5 类别、贮藏:参考 USP 现行标准和琥珀酸钠的用途,制订类别、贮藏项。
来源:药典委
原文下载:![]() 琥珀酸钠药用辅料标准草案公示稿.pdf
琥珀酸钠药用辅料标准草案公示稿.pdf
 咨询热线:400-888-1942
咨询热线:400-888-1942




